题目内容
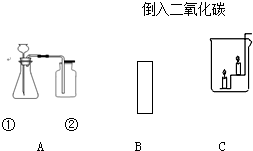 图中的A、B、C是实验室制取二氧化碳并探究其性质的装置和操作示意图,试回答下列问题:
图中的A、B、C是实验室制取二氧化碳并探究其性质的装置和操作示意图,试回答下列问题:(1)写出仪器①和②的名称,①是
锥形瓶
锥形瓶
,②是集气瓶
集气瓶
.(2)用稀盐酸和石灰石制取二氧化碳的化学方程式是
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(3)为了检验A装置的集气瓶里是否充满二氧化碳,可将燃着的木条放在
集气瓶口
集气瓶口
进行实验,如果火焰熄灭,证明已经充满.实验,如果火焰熄灭,证明已经充满.(4)在B 中通入二氧化碳,若B的试管里盛的是紫色石蕊试液,观察到的现象是
紫色石蕊试液变红
紫色石蕊试液变红
若该试管里盛的是澄清石灰水,观察到的现象是澄清石灰水变浑浊
澄清石灰水变浑浊
.(5)C所示的实验说明了二氧化碳不能燃烧,也不能支持燃烧的性质,同时也证明了二氧化碳的密度比空气的密度
大
大
.分析:(1)熟悉常见仪器,了解名称;
(2)熟记实验室制取二氧化碳的化学方程式;
(3)根据二氧化碳不燃烧也不支持燃烧进行解答;
(4)根据二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红以及能使澄清石灰水变浑浊进行解答;
(5)根据二氧化碳的密度比空气大进行解答.
(2)熟记实验室制取二氧化碳的化学方程式;
(3)根据二氧化碳不燃烧也不支持燃烧进行解答;
(4)根据二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红以及能使澄清石灰水变浑浊进行解答;
(5)根据二氧化碳的密度比空气大进行解答.
解答:解:(1)熟悉常见仪器,了解名称,①是锥形瓶,②是集气瓶;
(2)用稀盐酸和石灰石制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)二氧化碳不燃烧也不支持燃烧,为了检验A装置的集气瓶里是否充满二氧化碳,可将燃着的木条放在集气瓶口,如果火焰熄灭,证明已经充满;
(4)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红;二氧化碳能使澄清石灰水变浑浊;
(5)C所示的实验现象:下层的蜡烛先熄灭,上层的蜡后熄灭;说明了二氧化碳不能燃烧,也不能支持燃烧的性质;同时也证明了二氧化碳的密度比空气的密度大.
故答案为:(1)①是锥形瓶,②是集气瓶;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)集气瓶口;
(4)紫色石蕊试液变红;澄清石灰水变浑浊;
(5)大.
(2)用稀盐酸和石灰石制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)二氧化碳不燃烧也不支持燃烧,为了检验A装置的集气瓶里是否充满二氧化碳,可将燃着的木条放在集气瓶口,如果火焰熄灭,证明已经充满;
(4)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红;二氧化碳能使澄清石灰水变浑浊;
(5)C所示的实验现象:下层的蜡烛先熄灭,上层的蜡后熄灭;说明了二氧化碳不能燃烧,也不能支持燃烧的性质;同时也证明了二氧化碳的密度比空气的密度大.
故答案为:(1)①是锥形瓶,②是集气瓶;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)集气瓶口;
(4)紫色石蕊试液变红;澄清石灰水变浑浊;
(5)大.
点评:常见仪器的名称、实验室制取二氧化碳的化学方程式以及性质是我们经常的会遇到的问题,也是基础问题,同学们一定要掌握好.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
 超市中的许多食物用保鲜膜包装后出售.保鲜膜为什么可以“保鲜”呢?
超市中的许多食物用保鲜膜包装后出售.保鲜膜为什么可以“保鲜”呢?[查阅资料]保鲜膜除了可以阻止食物中水分流失,还能隔绝氧气及细菌,防止食物腐败.
[设计实验]在A、B、C三只相同的玻璃杯中,分别注入等体积的蒸馏水,并在各玻璃杯外壁标明刻度,如图所示放置一周.
【实验现象】一周后发现:A杯中水量几乎不变;C杯中
水量减少较多;B杯中水量减少不多;
【解 释】请用分子的知识解释C杯中水量减少的原因:
【提出问题1】制作保鲜膜的材料是热固性塑料还是热
塑性塑料呢?
【实 验】在一只试管中放入少量保鲜膜碎片,用酒精灯缓缓加热,观察到碎片熔化,冷却后变成固体,加热又可以熔化.由此得出:制作保鲜膜的材料是
(填“热塑性”或“热固性”)塑料.
【查阅资料】食物用保鲜膜使用的材料是聚乙烯.
【提出问题2】聚乙烯是由什么组成的?
【进行实验】兴趣小组的同学取了5.6克聚乙烯塑料碎片放在硬质玻璃管中,鼓入充足的氧气使之燃烧,将产生的气体通入足量的浓硫酸和氢氧化钠溶液中,并将实验结果记录在下表中:
| 实验前 | 实验后 | |
| B装置的 质量/g |
213.6 | 220.8 |
| C装置的 质量/g |
200.2 | 217.8 |
(2)由于聚乙烯中含有碳元素,有同学提出:如果不充分燃烧可能产生一氧化碳造成大气污染.于是化学兴趣小组的同学将上述装置进行修改,对聚乙烯塑料在空气中燃烧是否产生一氧化碳进行探究.
同学们查阅资料了解到:浸有磷钼酸溶液的氯化钯黄色试纸遇到微量CO,会立即变蓝;而该试纸遇CO2不变色.接着,化学兴趣小组在老师的指导下,修改上述装置(如下图),认真观察装置B、C的实验现象,
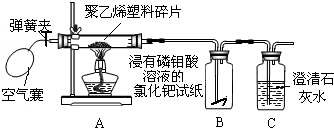
请你帮助他们完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 点燃酒精灯加热,随即打开弹簧夹,通入干燥的空气.观察装置B、C中的现象 | 装置B中的现象是: 装置C中的现象是: |
聚乙烯塑料在空气中燃烧,生成物中,既有CO2,也有CO.装置C中反应的化学方程式为: |

 ”粒子
”粒子 -碳原子
-碳原子