题目内容
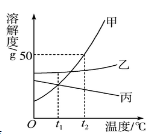
【题目】(8分)(1)下图是不与水发生化学反应的a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
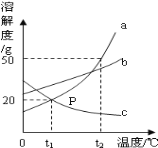
①P 点的含义是 。
②t 2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号)。
③t 2℃时30ga物质加入到50g水中不断搅拌,所得溶液的溶质质量分数 。
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号)。
A.c>a=b B.a=b>c C.a>b>c D.b>a>c
(2)根据下表回答:
OH- | NO3- | Cl- | SO42- | CO32- | |
H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Ca2+ | 微溶 | 溶 | 溶 | 微溶 | 不溶 |
Cu2+ | 不溶 | 溶 | 溶 | 溶 | 不溶 |
Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
Zn2+ | 不溶 | 溶 | 溶 | 溶 | 不溶 |
①BaCO3的溶解性 。从上表中找出一种不溶碱 (填化学式)。
②Zn(NO3)2、BaCl2两种溶液能不能发生反应? (填:能”或“不能”)
③利用上表写一个有氢氧化铜生成的复分解反应化学方程式: 。
【答案】(1)①温度为 t 1 ℃时 a 与 c 物质的溶解度相等 ②c<b<a ③33.3% ④D
(2)①不溶,Cu(OH)2 /Zn(OH)2 ; ②不能; ③2NaOH+CuCl2 ==2NaCl+Cu(OH)2↓
【解析】
试题分析:
(1)①由溶解度曲线可知,a 与 c相交于点p,故p点表示的是t 1 ℃时 a 与 c 物质的溶解度相等;
②由溶解度曲线可知,t 2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是c<b<a;
③t 2℃时a的溶解度为30g,即100g溶剂30ga恰好形成饱和溶液,那么50g溶剂中只能溶解25ga物质,故形成的溶液的质量为75g,溶质的质量分数=25/75 ×100%=33.3%;
④由溶解度曲线可知,a与b的溶解度随温度的升高而变大,故将t1℃时a、b、物质饱和溶液的温度升高到t2℃时溶液变成不饱和溶液,溶质的质量分数不变:b>a,而c的溶解度随温度的升高而减小,故升温后c溶液中有晶体析出,溶质的质量变小,故三种溶液的溶质质量分数大小关系是b>a>c;
(2)①由表格信息可知碳酸钡不溶于水;碱是由金属离子和氢氧根离子构成的,故难溶性碱是氢氧化铜和氢氧化锌;
②根据复分解反应发生的条件:两种化合物交换成分后的生成物中有水、气体或沉淀生成。故Zn(NO3)2、BaCl2两种溶液不能发生复分解反应;
③复分解反应是两种化合物交换成分生成另外两种化合物的反应,故要生成氢氧化铜沉淀,故是含有氢氧根离子的碱与含有铜离子的盐反应,故可以是氢氧化钠与氯化铜反应,生成的氯化钠和氢氧化铜沉淀:2NaOH+CuCl2 ==2NaCl+Cu(OH)2↓。

 名校课堂系列答案
名校课堂系列答案