题目内容
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2,CaCl2一级泥沙等杂质.为了有效将粗盐提纯,实验的个步骤操作流程如图所示.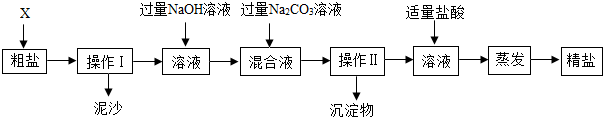
根据以上信息回答:
(1)操作Ⅰ和操作Ⅱ的名称是 ;操作Ⅱ后的沉淀物中含有的物质是 .
(2)判断加入的盐酸“适量”的方法是 .
(3)实验所得精盐的质量大于粗盐中NaCl的质量,原因是 .

根据以上信息回答:
(1)操作Ⅰ和操作Ⅱ的名称是
(2)判断加入的盐酸“适量”的方法是
(3)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
考点:氯化钠与粗盐提纯,过滤的原理、方法及其应用,盐的化学性质
专题:常见的盐 化学肥料
分析:(1)操作Ⅰ和操作Ⅱ是将泥沙、不溶物与溶液分离;氢氧化钠溶液和氯化镁反应生成的氢氧化镁白色沉淀,碳酸钠溶液和氯化钙溶液反应生成的碳酸钙白色沉淀;据此进行分析解答.
(2)盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳气体,据此进行分析解答.
(3)根据除去氯化镁和氯化钙杂质,以及除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠,进行分析解答.
(2)盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳气体,据此进行分析解答.
(3)根据除去氯化镁和氯化钙杂质,以及除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠,进行分析解答.
解答:解:(1)操作Ⅰ和操作Ⅱ是将泥沙、不溶物与溶液分离,为过滤操作;
氢氧化钠溶液和氯化镁反应生成的氢氧化镁白色沉淀和氯化钠,碳酸钠溶液和氯化钙溶液反应生成的碳酸钙白色沉淀和氯化钠,故操作Ⅱ后的沉淀物有:氢氧化镁和碳酸钙.
(2)盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳气体,滴加至刚好不再产生气泡时,稀盐酸和氢氧化钠、碳酸钠恰好完全反应
(3)除去氯化镁和氯化钙杂质,以及除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠,所以实验所得精盐的质量大于粗盐中NaCl的质量
故答案为:(1)过滤;氢氧化镁和碳酸钙;(2)刚好不再产生气泡;(3)除去氯化镁和氯化钙杂质、除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠.
氢氧化钠溶液和氯化镁反应生成的氢氧化镁白色沉淀和氯化钠,碳酸钠溶液和氯化钙溶液反应生成的碳酸钙白色沉淀和氯化钠,故操作Ⅱ后的沉淀物有:氢氧化镁和碳酸钙.
(2)盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳气体,滴加至刚好不再产生气泡时,稀盐酸和氢氧化钠、碳酸钠恰好完全反应
(3)除去氯化镁和氯化钙杂质,以及除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠,所以实验所得精盐的质量大于粗盐中NaCl的质量
故答案为:(1)过滤;氢氧化镁和碳酸钙;(2)刚好不再产生气泡;(3)除去氯化镁和氯化钙杂质、除去过量的氢氧化钠和碳酸钠溶液的过程中都生成了氯化钠.
点评:本题难度不大,掌握粗盐提纯的原理、盐的化学性质、酸的化学性质等是正确解答本题的关键.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
为减少煤燃烧带来的大气污染,提高煤的燃烧效率,一些城市使用焦炉煤气(焦炉煤气是脱硫煤隔绝空气强热的部分产物)作为洁净的生活燃料.以下实验流程是对焦炉煤气的成分进行局部探究,下列结论中错误的是( )
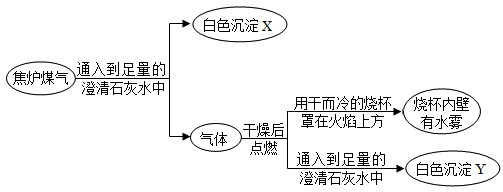

| A、焦炉煤气中一定含有二氧化碳 |
| B、X、Y都是碳酸钙 |
| C、焦炉煤气中可能含有H2和CH4或只有CH4 |
| D、焦炉煤气是CO和其他气体的混合物 |
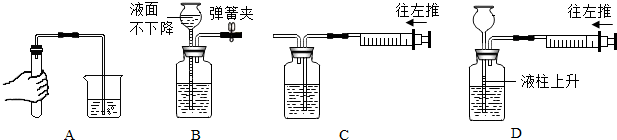
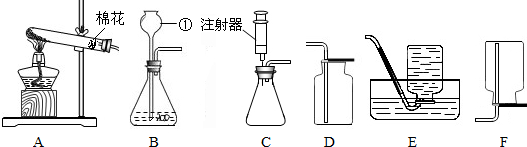
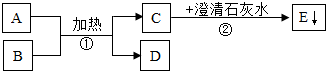 已知A、C为无色气体,B为黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答:
已知A、C为无色气体,B为黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答: