题目内容
根据如图所示制取气体的装置,回答下列问题(装置选择填序号):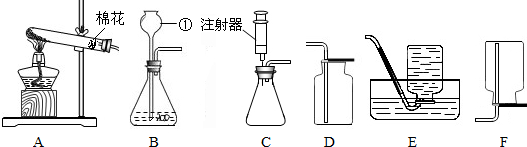
(1)实验仪器①的名称是 .
(2)用高锰酸钾制取氧气时,反应的化学方程式为 ,所选用的发生装置是 ,若收集干燥的氧气应选用的装置是 ,验满的方法是 .
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,我认为选用C的优点是 .将注射器换成 (填实验室常用仪器)也有同样的效果.
(4)用大理石和稀盐酸制取二氧化碳时,可选取B装置作发生装置,检查B装置气密性的方法是 ;若装置B中反应剧烈,从实验安全角度考虑,可以采取的措施有 (填序号).
①用容积较小的锥形瓶 ②减慢液体的加入速率
③加热反应物 ④降低液体反应物的浓度.

(1)实验仪器①的名称是
(2)用高锰酸钾制取氧气时,反应的化学方程式为
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,我认为选用C的优点是
(4)用大理石和稀盐酸制取二氧化碳时,可选取B装置作发生装置,检查B装置气密性的方法是
①用容积较小的锥形瓶 ②减慢液体的加入速率
③加热反应物 ④降低液体反应物的浓度.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,氧气的检验和验满,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)据常用仪器回答;
(2)据反应原理书写方程式,高锰酸钾制取氧气需要加热,故选发生装置A,收集干燥的氧气应用排空气法,验满氧气的方法是将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(3)C装置中的注射器可以控制反应物的量,从而控制反应速率,分液漏斗也具有此用途;
(4)据检查气密性的方法分析解答,要控制反应速率,则须控制反应物的量或减小浓度.
(2)据反应原理书写方程式,高锰酸钾制取氧气需要加热,故选发生装置A,收集干燥的氧气应用排空气法,验满氧气的方法是将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(3)C装置中的注射器可以控制反应物的量,从而控制反应速率,分液漏斗也具有此用途;
(4)据检查气密性的方法分析解答,要控制反应速率,则须控制反应物的量或减小浓度.
解答:解:(1)标号仪器是长颈漏斗;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4
K2MnO4+MnO2+O2↑;该反应需要加热,故选发生装置A,氧气的密度比空气大,所以收集干燥的氧气应用向上排空气法,验满氧气的方法是将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(3)C装置中的注射器可以控制反应物的量,从而控制反应速率,分液漏斗也具有此用途;
(4)检查B装置气密性的方法是:向长颈漏斗中加少许水,封住漏斗下口,将导气管伸入水中,用手紧握锥形瓶,若导管口出现气泡,松口手导管口形成一段水柱,则气密性良好;
要控制反应的剧烈程度,可采取的措施是:减慢液体的滴加速度可以使反应速率减慢;反应物浓度越小,反应速率越慢.不选用的措施是用容积较小的锥形瓶,对反应速率无影响,且有危险,加热反应物会使反应速率加快,不可取;
故答案为:(1)长颈漏斗;
(2)2KMnO4
K2MnO4+MnO2+O2↑; A; D; 将带火星的木条放在集气瓶口,木条复燃,则氧气已满;
(3)可以控制反应速率; 分液漏斗;
(4)向长颈漏斗中加少许水,封住漏斗下口,将导气管伸入水中,用手紧握锥形瓶,若导管口出现气泡,松口手导管口形成一段水柱,则气密性良好(合理均可); ②④.
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是:2KMnO4
| ||
(3)C装置中的注射器可以控制反应物的量,从而控制反应速率,分液漏斗也具有此用途;
(4)检查B装置气密性的方法是:向长颈漏斗中加少许水,封住漏斗下口,将导气管伸入水中,用手紧握锥形瓶,若导管口出现气泡,松口手导管口形成一段水柱,则气密性良好;
要控制反应的剧烈程度,可采取的措施是:减慢液体的滴加速度可以使反应速率减慢;反应物浓度越小,反应速率越慢.不选用的措施是用容积较小的锥形瓶,对反应速率无影响,且有危险,加热反应物会使反应速率加快,不可取;
故答案为:(1)长颈漏斗;
(2)2KMnO4
| ||
(3)可以控制反应速率; 分液漏斗;
(4)向长颈漏斗中加少许水,封住漏斗下口,将导气管伸入水中,用手紧握锥形瓶,若导管口出现气泡,松口手导管口形成一段水柱,则气密性良好(合理均可); ②④.
点评:此题具有很强的综合性,涉及了实验装置的选取,反应速度的控制等知识点.解题的关键在于充分的利用图示,正确的结合实验操作技能排除干扰项,定能迎刃而解.

练习册系列答案
相关题目
实验室用98%的浓硫酸(密度1.84g/cm3)配制一定溶质质量分数的稀硫酸,不需要的仪器是( )
| A、玻璃棒 | B、量筒 |
| C、烧杯 | D、托盘天平 |

 小冰将一定量的铁粉加入硝酸银溶液,充分反应后想进行过滤操作后继续实验,判断反应情况.
小冰将一定量的铁粉加入硝酸银溶液,充分反应后想进行过滤操作后继续实验,判断反应情况.