题目内容
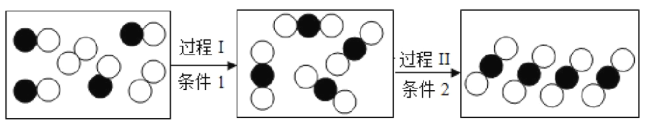
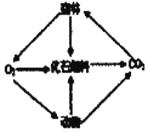
【题目】新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如图所示:
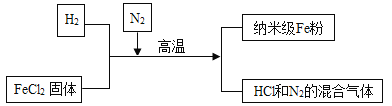
请回答下列问题:
(1)上述流程中可以循环利用的物质是______,在制备纳米级Fe粉的工艺流程中,其作用是______。
(2)纳米级Fe粉在氧气中能自发燃烧生成黑色固体,该反应的化学方程式为______。
(3)上述制备纳米级铁粉的化学方程式是______,其反应类型为______。
(4)研究人员发现最后在制得的纳米级Fe粉样品中混有少量的![]() 杂质,为了除去样品中的杂质,在无氧环境下,先加水溶解,然后再洗涤、______、烘干。
杂质,为了除去样品中的杂质,在无氧环境下,先加水溶解,然后再洗涤、______、烘干。
【答案】![]() 保护气,防止铁粉氧化
保护气,防止铁粉氧化 ![]()
![]() 置换反应 过滤
置换反应 过滤
【解析】
(1)由工艺流程图可知,氮气是可以回收利用的,因为氮气没有参加反应,在制备过程中,是利用了氮气的化学性质稳定,用来作保护气,防止铁粉氧化;
(2)铁在氧气中燃烧生成黑色固体四氧化三铁,其方程式为:![]()
(3)在高温的条件下,氢气与氯化亚铁反应生成铁和氯化氢,该反应是由单质与化合物反应生成另一种单质与另一种化合物,属于置换反应;
(4)铁不溶于水,氯化亚铁溶于水,所以加水溶解,再进行过滤、洗涤干燥即可;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目