题目内容
(7分)将2.34gNaCl固体溶于103.4g水中得到不饱和溶液,再向所得溶液中小心滴入200g AgNO3溶液。实验过程中,生成的AgCl的质量与滴入的AgNO3 溶液的质量关系如下图所示(提示:NaCl + AgNO3 =" AgCl↓+" NaNO3)。
溶液的质量关系如下图所示(提示:NaCl + AgNO3 =" AgCl↓+" NaNO3)。
(1)计算A点处生成NaNO3的质量?
(2)计算B点溶液中AgNO3的溶质质量分数?
(若最后结果不能整除,保留小数点后一位)
(7分)(1)解:设A点处生成NaNO3的质量为x
AgNO3 + NaCl =" AgCl↓" + NaNO3
58.5 85
2.34g x =
=
x = 3.4g
(2)设A点处反应AgNO3的质量为y,生成AgCl的质量为z
AgNO3 + NaCl =" AgCl↓" + NaNO3
170 58.5 143.5
y 2.34g z 
m(B点溶液)="2.34g" +103.4g + 200g - 5.74g = 300g
B点溶液AgNO3的溶质质量分数 = × 100% = 2.3%
× 100% = 2.3%
(其他合理解答参照给分)
答:A点处生成NaNO3的质量为3.4g,B点溶液AgNO3的溶质质量分数为2.3%。
解析

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目
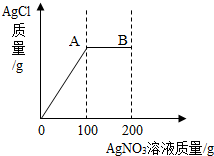 将2.34gNaCl固体溶于103.4g水中得到不饱和溶液,再向所得溶液中小心滴入200g AgNO3溶液.实验过程中,生成的AgCl的质量与滴入的AgNO3溶液的质量关系如图所示(提示:NaCl+AgNO3=AgCl↓+NaNO3 ).
将2.34gNaCl固体溶于103.4g水中得到不饱和溶液,再向所得溶液中小心滴入200g AgNO3溶液.实验过程中,生成的AgCl的质量与滴入的AgNO3溶液的质量关系如图所示(提示:NaCl+AgNO3=AgCl↓+NaNO3 ).

