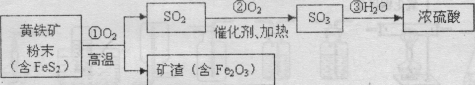
题目内容
【题目】(7分)已知固体混合物A是由KCl、KNO3、CaCO3三种物质中的两种组成;另有一固体混合物B是由NH4Cl、CuO、CuCl2三种物质中的两种组成。按下图所示进行实验,出现的现象如图中所示(设过程中所有发生的反应都恰好完全进行):
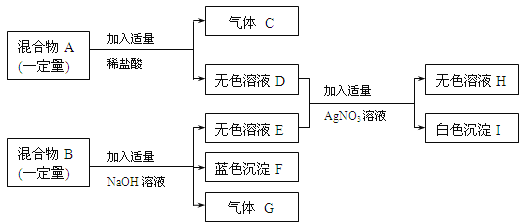
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)沉淀F的化学式为_____________。
(2)气体C和气体G中能使湿润的红色石蕊试纸变蓝的气体是 (填“C”或“G”)。
(3)混合物B的组成是 (填物质的化学式)。
(4)无色溶液H中一定含有 种溶质。
(5)写出1个生成白色沉淀I的化学方程式 。
(6)如果要确定固体混合物A的组成,还需取少量混合物A再进行实验,请简要说明实验操作步骤、发生的现象及结论: 。
【答案】(1) Cu(OH)2 (2) G (3) NH4Cl、CuCl2。(4)3 (5)NaCl+AgNO3=AgCl↓+NaNO3或CaCl2+2AgNO3=2AgCl↓+Ca(NO3)2 (6)取少量固体A于试管中,加水充分溶解后过滤,再向滤液中加入足量的硝酸银溶液。若产生白色沉淀,则混合物A由KCl和CaCO3组成;若不产生白色沉淀,则混合物A由KNO3和CaCO3组成
【解析】
试题分析:根据酸碱盐的性质,混合物A中加入稀盐酸,产生气体C为二氧化碳,说明含有碳酸钙;混合物B,加入氢氧化钠溶液产生气体G为氨气;说明混合物B中一定含有氯化铵;产生蓝色沉淀,说明一定含有氯化铜;一定不含氧化铜;无色溶液E中一定含有氯离子,故(1)沉淀F的化学式为Cu(OH)2 ;(2)气体C和气体G中能使湿润的红色石蕊试纸变蓝的气体是G氨气;(3)混合物B的组成是NH4Cl、CuCl2(4)无色溶液H中一定含有3种溶质硝酸钾、硝酸钙、硝酸钠;(5)1个生成白色沉淀I的化学方程式NaCl+AgNO3=AgCl↓+NaNO3或CaCl2+2AgNO3=2AgCl↓+Ca(NO3)2;(6)如果要确定固体混合物A的组成,还需取少量混合物A再进行实验,具体操作为取少量固体A于试管中,加水充分溶解后过滤,再向滤液中加入足量的硝酸银溶液。若产生白色沉淀,则混合物A由KCl和CaCO3组成;若不产生白色沉淀,则混合物A由KNO3和CaCO3组成

 导学教程高中新课标系列答案
导学教程高中新课标系列答案【题目】某品牌可乐由水、白砂糖、焦糖色素(使可乐显黑褐色)、磷酸(H3PO4)等,按一定比例混合并压入二氧化碳配制而成。某同学为了探究可乐的成分及其含量,进行如下实验。
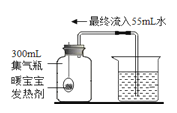
实验一 可乐中二氧化碳的定性检验
(1)请完成下表:
实验步骤 | 实验现象 | 结论 |
打开一塑料瓶装可乐,塞上带导管的橡胶塞,把导管插入 (填化学式)溶液中 | 观察到 | 可乐中含有二氧化碳 |
实验二 可乐中磷酸的定量测定
测定过程如下:
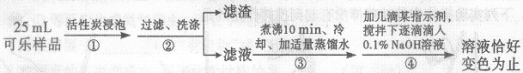
(2)步骤①用活性炭浸泡的目的是 。
(3)步骤③煮沸10分钟的目的是除尽滤液中的 。
(4)已知步骤④反应的化学方程式为H3PO4+NaOH=NaH2PO4+H2O,测得共消耗0.1%的NaOH溶液20g,忽略可乐中其它成分对测定结果的影响,计算可乐中磷酸的含量(以g/L为单位。相对分子质量:H3PO4—98;NaOH—40),写出计算过程。
(5)如果步骤②缺少洗涤,则测定结果 (填“偏高”“不变”或“偏低”)。
【题目】除去下列各物质中的少量杂质,所用方法不可行的是
选项 | 物质 | 杂质 | 除去杂质的方法 |
A | Cu粉 | Fe粉 | 用磁铁吸出 |
B | NaCl | 泥沙 | 加水溶解、过滤、蒸发 |
C | NaOH | Na2CO3 | 滴入足量稀盐酸至不再产生气泡 |
D | O2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |