题目内容
【题目】实验室中有一包白色固体是由氯化钠、氯化钡、硫酸铜、碳酸钠中的两种或两种以上的物质组成。某课外活动小组对这包白色固体进行了如下的探究实验:(假设下面各步都刚好完全反应)
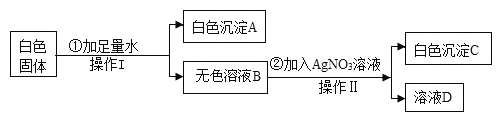
根据上述实验回答下列问题:
(1)玻璃棒在操作Ⅰ、Ⅱ中的作用是___________________________________________。
(2)白色固体中可能含有_________________,写出步骤①中发生反应的化学方程式_______
(3)白色沉淀C为______________________________。
【答案】引流 氯化钠(NaCl) BaCl2+Na2CO3=BaCO3↓+2NaCl 氯化银(AgCl)
【解析】
硫酸铜在溶液中显蓝色,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,氯离子和银离子反应生成氯化银沉淀,白色固体加水溶解,得到白色沉淀和溶液B,溶液B中加入硝酸银,得到白色沉淀C和溶液D,所以B中一定含有氯离子,C是氯化银沉淀,所以
(1)玻璃棒在操作Ⅰ、Ⅱ中的作用是:引流;
(2)氯化钡和碳酸钠反应生成氯化钠和碳酸钡,白色固体中可能含有氯化钠,步骤①中发生的反应是碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)白色沉淀C为氯化银。
故答案为:(1)引流;
(2)氯化钠;BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)氯化银。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】 “ ”是重要的化学学科思想。请根据提供的信息,填写表中相对应的内容。
”是重要的化学学科思想。请根据提供的信息,填写表中相对应的内容。
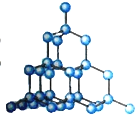
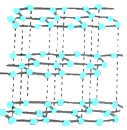
物质 | 金刚石 | 石墨 | 木炭 | 炭黑 |
结构 |
|
| ③_____ (填文字) |
碳原子 |
性质 | ①_____ | 质软、滑腻感 | 吸附性 | ④_____ |
用途 | 裁玻璃、切割大理 石、做钻头等 | ②_____ | 吸附剂 | 制墨,用于书写的字长期保存不褪色 |