题目内容
【题目】我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。流程简图如下
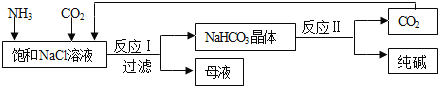
(已知:氨气极易溶于水。母液中有一种物质是NH4Cl) ,下列有关说法错误的是
A. 反应中先通入氨气的目的是促进二氧化碳的吸收,提高产率
B. 反应II得到的CO2可以循环使用
C. 反应I的方程式为NaCl+NH3+CO2 =NaHCO3↓+NH4Cl
D. “母液”中一定只含有两种溶质
【答案】D
【解析】A、氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故正确;
B、二氧化碳在反应中能循环利用,故正确;
C、沉淀池中发生反应的反应物是氯化钠、氨气、二氧化碳和水,生成的是碳酸氢钠和氯化铵,方程式为:NaCl+NH3+CO2═NaHCO3↓+NH4Cl,故正确;
D、过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故错误。

 天天向上口算本系列答案
天天向上口算本系列答案【题目】同学们运用对比的学习方法探究碱的性质。
实验一 | 实验二 |
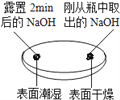
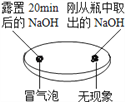
观察固体表面
| 向两块固体表面滴加稀盐酸
|
(1)由上图实验一、二可知,氢氧化钠会吸收空气的_________,因此要密封保存。
(2)同学们看到盛有NaOH的试剂瓶上标注着“NaOH含量不少于96.0%”,开始如下探究:
【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】工业制取NaOH的反应原理是:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质为_________和NaCl。理由是氢氧化钠暴露在空气中变质和氯化钠没有完全转化为氢氧化钠。
【实验探究】取样溶于水,并分成两份。
实验步骤 | 实验现象 | 实验结论 |
步骤①:向一份溶液中滴加酚酞试剂 | 溶液变红 | 猜想正确 |
步骤②:向另一份溶液中滴加过量___________ | 产生气泡 | |
步骤③:向步骤②所得溶液中滴加___________溶液 | 产生白色沉淀 |
【实验反思】
Ⅰ.上述实验中步骤 ___(填写序号)是没有必要进行的;
Ⅱ.步骤②所得溶液中的溶质除NaCl外,还有____________。