题目内容
【题目】如图是氢氧化钠溶液与硫酸溶液反应时的溶液pH变化示意图,请判断下列说法正确的是( )
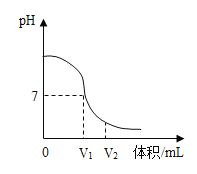
A.根据图示判断,该实验是将氢氧化钠溶液滴加到硫酸溶液中
B.滴入溶液体积为V2mL时,溶液中的离子为H+和SO42-
C.滴入溶液体积为V1mL时,溶液中的溶质为硫酸钠
D.滴入溶液体积为V1mL时,硫酸溶液中的H+和氢氧化钠溶液中的OH-恰好完全反应生成水
【答案】CD
【解析】
A. 根据图示溶液的pH变小可判断,该实验是将硫酸溶液滴加到氢氧化钠溶液中,选项错误;
B. 滴入溶液体积为V2mL时,溶液的pH小于7,可知酸过量,溶液中的溶质为硫酸钠和硫酸,离子为H+和SO42-,Na+,选项错误;
C. 滴入溶液体积为V1mL时,溶液的pH=7,说明硫酸和氢氧化钠刚好完全反应,溶液中溶质只有硫酸钠,选项正确;
D. 中和反应的实质是氢离子和氢氧根离子生成水分子,滴入溶液体积为V1mL时,硫酸溶液中的H+和氢氧化钠溶液中的OH-恰好完全反应生成水,选项正确。
故选CD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】探究纯碱成分。我国科学家侯德榜在氨碱法的基础上创立了候氏制碱法,其生产流程简明如下图:
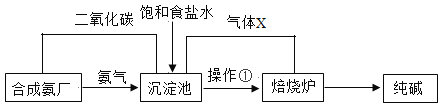
请根据流程图回答下面问题:
(1)写出沉淀池中发生反应的化学方程式___________。
(2)上述流程中气体X的化学式是___________
(3)沉淀池中晶体转移至熔烧炉时用到操作①,操作①的名称是____________。
(4)用“侯氏制碱法”制得的纯碱中可能含有碳酸氢钠、氯化钠等杂质,化学兴趣小组对某品牌纯碱样品的成分及含量进行了实验探究
(定性实验)探究样品的成分
实验步骤 | 实验现象 | 实验结论. |
_______ | _______ | 样品中不含碳酸氢钠 |
_______ | _______ | 样品中含有氯化钠 |
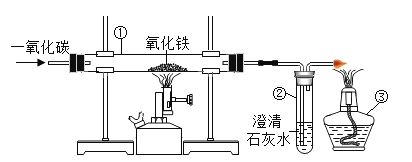
(定量实验)利用样品与稀盐酸反应,测定Na2CO3的质量分数。实验装置(铁架台略去)如下图所示。(装置气密性良好,忽略盐酸的挥发性且每步反应成作用都是完全的)。
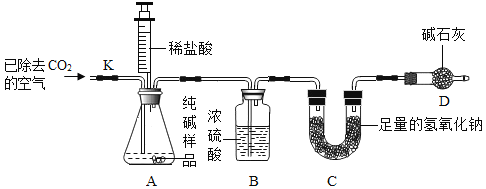
实验步骤:
1检查装置的气密性,将6g纯碱样品放入锥形瓶中
2称量反应前C装置质量为50g
3组装装置,用注射器向A中加入50mL稀盐酸时,A中不再产生气泡。
4打开止水夹K,通入已除去CO2的空气,一段时间后关闭止水夹
5称量装置C反应后的质量为52.2g
(5)①评价方案:步骤4的作用是______________,缺少装置B,将会使测定结果____________(选填“偏大”成“偏小“或“不变”).
②根据题中的数据计算纯碱样品中碳酸钠的质量分数为____________(计算结果精确到0.1%)。
【题目】(1)热水瓶用久后,瓶胆内壁常附着一层水垢,老师说其成分主要是碳酸钙、碳酸氢钙、氢氧化镁等。小组同学认为可使用稀盐酸除去,请写出发生中和反应的化学方程式________________________。
日常生活中,每位同学都会接触到硬水。某校化学兴趣小组的同学在老师的带领下对硬水进行了一些探究和拓展实验。
(查阅资料)水的硬度是由水中溶解的可溶性钙和镁化合物引起的,硬水中溶解的钙和镁化合物可分为两类:钙、镁的碳酸氢盐:钙、镁的硫酸盐或氯化物,一般所说的水的硬度是由上述两类化合物引起的。
(2)小组同学对硬水中为什么含有碳酸氢钙非常感兴趣,于是再次学习九年级化学下册课本中的资料卡片:石笋和钟乳石的形成。知道了当石灰岩遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O=Ca(HCO3)2小组同学思考:若向碳酸钠溶液中通入一定量的二氧化碳,是否也能生成碳酸氢钠?
于是他们对此开始实验探究(不考虑二氧化碳和碳酸作为溶质的情况)。
(提出问题)所得溶液中溶质是什么?
(提出猜想)
猜想一:溶质为Na2CO3;
猜想二:溶质为 NaHCO3;
猜想三:溶质为___________。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
a.__________________________。 | 有白色沉淀生成 | 猜想二_________________ (填“成立”或“不成立”) |
b.取实验步骤a中上层清液,滴 加适量稀盐酸 | 有气泡冒出 | 猜想一不成立 |
写出实验步骤b中发生反应的化学方程式_____________________。
通过实验,小组同学得出了正确结论。
(拓展)氢氧化钠溶液中通入过量二氧化碳气体,反应的化学方程式为__________。