题目内容
【题目】用右图所示装置,
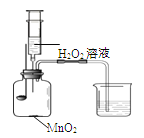
在常温下分别进行研究燃烧条件和研究氧气性质的实验。
已知:白磷的着火点为40℃。

(1)H2O2稀溶液与MnO2接触时,发生反应的化学方程式为 。
(2) 实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是 ;推入H2O2溶液后,观察到烧杯中的现象是 。
(3)实验2中, 推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是 ;木炭由燃烧到熄灭再到集气瓶冷却一段时间的过程中,烧杯中的实验现象是 。
【答案】(1)2H2O2![]() 2H2O +O2↑
2H2O +O2↑
(2)温度未达到白磷着火点,白磷未与氧气接触 ;白磷燃烧
(3)支持燃烧;石灰水变浑浊,部分液体被吸入集气瓶中
【解析】
试题分析:H2O2稀溶液与MnO2接触时,发生反应的化学方程式为2H2O2![]() 2H2O +O2↑; 实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是温度未达到白磷着火点,白磷未与氧气接触 ;推入H2O2溶液后,观察到烧杯中的现象是白磷燃烧;实验2中, 推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭由燃烧到熄灭再到集气瓶冷却一段时间的过程中,烧杯中的实验现象是石灰水变浑浊,部分液体被吸入集气瓶中,因为过程中瓶内的气压会降低。
2H2O +O2↑; 实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是温度未达到白磷着火点,白磷未与氧气接触 ;推入H2O2溶液后,观察到烧杯中的现象是白磷燃烧;实验2中, 推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭由燃烧到熄灭再到集气瓶冷却一段时间的过程中,烧杯中的实验现象是石灰水变浑浊,部分液体被吸入集气瓶中,因为过程中瓶内的气压会降低。

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目

