题目内容
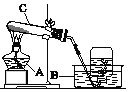
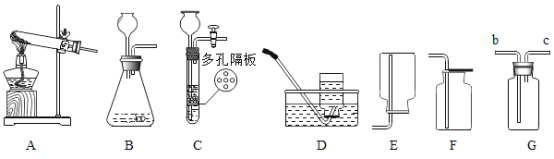
【题目】在学生完成“实验活动1氧气的实验室制取与性质”后,吴老师发现部分小组制取氧气后的试管内还有暗紫色固体。吴老师称得某实验小组剩余固体的质量为9.36g,经溶解过滤、洗涤、烘干后所得黑色固体的质量为1.74g。请计算:
(1)高锰酸钾中锰元素和氧元素的质量比是___。
(2)生成氧气的质量___
(3)该实验小组高锰酸钾的分解率___。
(查阅资料)
(1)含钾元素的化合物都能溶于水
(2)分解率=![]() ×100%
×100%
【答案】高锰酸钾中锰元素和氧元素的质量比是55:64 生成氧气的质量为0.64g 该实验小组高锰酸钾的分解率为63.2%
【解析】
(1)根据高锰酸钾的化学式KMnO4,可以计算中锰元素、氧元素的质量比=55:(16×4)=55:64。
(2)对应物质中只有二氧化锰不溶于水且是黑色固体,所以1.74g为二氧化锰。
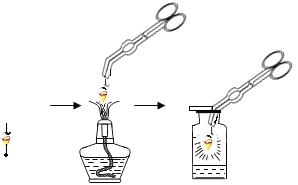
设生成的氧气的质量为x,分解的高锰酸钾的质量为y,生成的锰酸钾的质量为z
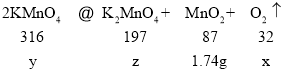
![]()
x=0.64g,y=6.32g,z=3.94g
则没分解的高锰酸钾的质量为9.36g﹣1.74g﹣3.94g=3.68g
则该实验小组高锰酸钾的分解率为![]()
(1)高锰酸钾中锰元素和氧元素的质量比是55:64;
(2)生成氧气的质量为0.64g;
(3)该实验小组高锰酸钾的分解率为63.2%。

【题目】甲、乙两个化学兴趣小组分别利用实验桌上的氢氧化钠溶液和稀盐酸进行实验。甲组同学将一定量稀盐酸滴入氢氧化钠溶液中,未能观察到明显现象,于是进行了如下探究:
实验一:探究氢氧化钠和稀盐酸是否能发生反应。
序号 | 实验操作 | 实验现象 | 实验结论 |
1 | 取滴加稀盐酸后的溶液样品于试管中,滴加酚酞溶液 | 溶液变红色 | 氢氧化钠与稀盐酸不反应 |
2 | 取滴加稀盐酸后的溶液样品于试管中,加入锌粒 | 现象A | 氢氧化钠与稀盐酸发生反应 |
(1)现象A为:_________。
(2)对于不同的实验结果,小组经讨论认为实验_______(填“1”或“2”)不严谨,理由是:_______。
乙组同学将稀盐酸滴入另一份未盖好瓶塞的氢氧化钠溶液中实验时,观察到有气泡产生这一反常现象,他们得出该氢氧化钠已变质。
实验二:测定该氢氧化钠溶液中碳酸钠的质量分数。
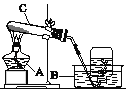
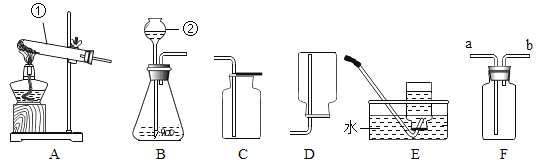
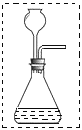
他们在老师的帮助下设计了如图装置进行实验。实验中样品质量为M克,最后测得实验后C瓶质量增加了N克,根据M、N,可计算得出该样品中碳酸钠的质量分数。

(3)氢氧化钠溶液在空气中变质的原因是_________。
(4)若没有B装置,则测出的碳酸钠质量分数将________(填“偏大”、“偏小”或“不变”)
(5)实验中,待A中反应结束后,需通入充足氮气,该操作的目的是________。