题目内容
下列图象与所述实验相符的是( )
A、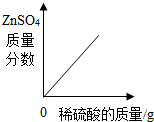 向一定量锌粒中加入过量稀硫酸 |
B、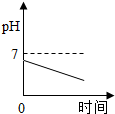 向一定量的稀硫酸中加入足量的锌粒 |
C、 向pH=2的溶液中加入碱性溶液 |
D、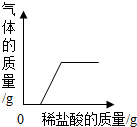 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 |
考点:金属的化学性质,酸的化学性质,中和反应及其应用
专题:元素化合物知识型
分析:A、向一定量锌粒中加入过量稀硫酸,随稀硫酸的不断加入,反应后所得溶液中硫酸锌的质量分数不断增大,至完全反应后硫酸锌质量不再增加,但因为溶液的质量不断增加,硫酸锌溶液的质量分数将慢慢减小,因为溶液的质量随着稀硫酸的不断加入而不断增加,而硫酸锌的质量不再增加,所以硫酸锌溶液的质量分数应该会慢慢减小(但不会到零);
B、根据锌与稀硫酸的反应,分析硫酸的质量分数与加入的锌的质量关系分析;
C、向酸溶液中不断的滴加碱溶液时,由于酸碱中和,会使溶液的酸性逐渐的减弱直至为中性或变为碱性;
D、在NaOH和碳酸钠的混合溶液中,逐滴加入稀盐酸,开始是先与氢氧化钠反应不会生成气体.
B、根据锌与稀硫酸的反应,分析硫酸的质量分数与加入的锌的质量关系分析;
C、向酸溶液中不断的滴加碱溶液时,由于酸碱中和,会使溶液的酸性逐渐的减弱直至为中性或变为碱性;
D、在NaOH和碳酸钠的混合溶液中,逐滴加入稀盐酸,开始是先与氢氧化钠反应不会生成气体.
解答:解:
A、图象表明,随稀硫酸质量的增加,生成的硫酸锌溶液的溶质质量分数逐渐增大;至完全反应后硫酸锌质量不再增加,但因为溶液的质量不断增加,硫酸锌溶液的质量分数将慢慢减小“,因为溶液的质量随着稀硫酸的不断加入而不断增加,而硫酸锌的质量不再增加,所以硫酸锌溶液的质量分数应该会慢慢减小(但不会到零).故A错误;
B、向一定量的锌粒中加入稀硫酸时,硫酸的质量的会越来越少,最终溶液的PH增大,但不会大于7.故B错误;
C、由于滴加的氢氧化钠溶液是过量的,因此最终溶液的PH应该大于7,故B错误;
D、在NaOH和碳酸钠的混合溶液中,逐滴加入稀盐酸,开始是先与氢氧化钠反应不会生成气体,故此选项正确.
故选:D.
A、图象表明,随稀硫酸质量的增加,生成的硫酸锌溶液的溶质质量分数逐渐增大;至完全反应后硫酸锌质量不再增加,但因为溶液的质量不断增加,硫酸锌溶液的质量分数将慢慢减小“,因为溶液的质量随着稀硫酸的不断加入而不断增加,而硫酸锌的质量不再增加,所以硫酸锌溶液的质量分数应该会慢慢减小(但不会到零).故A错误;
B、向一定量的锌粒中加入稀硫酸时,硫酸的质量的会越来越少,最终溶液的PH增大,但不会大于7.故B错误;
C、由于滴加的氢氧化钠溶液是过量的,因此最终溶液的PH应该大于7,故B错误;
D、在NaOH和碳酸钠的混合溶液中,逐滴加入稀盐酸,开始是先与氢氧化钠反应不会生成气体,故此选项正确.
故选:D.
点评:在处理图象类问题时,曲线的起点、折点及变化趋势是分析曲线的重要依据.

练习册系列答案
相关题目
下列变化中,不包含化学变化的是( )
| A、汽油挥发 | B、钢铁生锈 |
| C、煤燃烧 | D、牛奶变酸 |
下列清洗方法利用了乳化原理的是( )
| A、用稀盐酸清洗久置石灰水的试剂瓶 |
| B、用酒精清洗残留碘的试管 |
| C、用洗洁精清洗餐具上的油污 |
| D、用汽油清洗粘在手上的油漆 |
乙醇汽油是在汽油中加入适量酒精混合而成的一种燃料.乙醇(用X表示)完全燃烧的化学方程式为X+3O2
2CO2+3H2O.推断乙醇的化学式为( )
| ||
| A、C2H6O |
| B、C3H8 |
| C、C2H6 |
| D、C4H6O2 |
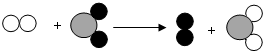 已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图(说明:一种小球代表一种元素的原子),则下列说法中正确的是( )
已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图(说明:一种小球代表一种元素的原子),则下列说法中正确的是( )| A、图中的反应物都是化合物 |
| B、该反应属于置换反应 |
| C、该反应属于复分解反应 |
| D、该反应前后出现了四种元素 |
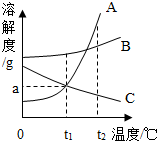 如图为A、B、C三种固体物质的溶解度曲线.据图回答下列问题.
如图为A、B、C三种固体物质的溶解度曲线.据图回答下列问题.