题目内容
20°C时,某物质的溶解度为30g,把该物质50g溶于150g水中,所得溶液的质量为( )
| A、200g | B、195g |
| C、180g | D、80g |
考点:固体溶解度的概念
专题:溶液、浊液与溶解度
分析:首先判断形成的溶液是否饱和,由这一温度下的溶解度计算知道100g水最多可溶解30g该物质,所以制得的溶液为饱和溶液.
解答:解:已知20℃时,该物质的溶解度为30克,此温度下该物质50克放入150克的水中充分溶解后,只能溶解45g溶质,该溶液为饱和溶液,溶液质量=150g+45g=195g;
故答案为:B.
故答案为:B.
点评:此题考查了溶液饱和与不饱和状态的判断,掌握了饱和溶液的溶质质量分数的计算.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
下列区分物质的方法错误的是( )
| A、用肥皂水可区分硬水与软水 |
| B、用燃烧法可以区分羊毛和尼龙线 |
| C、用酚酞溶液区分蒸馏水和稀盐酸 |
| D、用水可以区分氢氧化钠固体与硝酸铵固体 |
下图所示的实验操作正确的是( )
A、 |
B、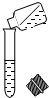 |
C、 |
D、 |
碱溶液具有许多相似的化学性质,这是因为碱溶液中都含有( )
| A、氢离子 | B、金属离子 |
| C、氢氧根离子 | D、酸根离子 |
有X、Y、Z三种金属,Y、Z分别放入稀硫酸中,Y溶解、Z不溶解;将Z放入XSO4的溶液中,Z的表面有X析出.则X、Y、Z三种金属的活动性由强到弱的是( )
| A、X>Y>Z |
| B、Y>Z>X |
| C、Y>X>Z |
| D、X>Z>Y |
在室温时,将1g葡萄糖放入100g水中,充分搅拌后,配成水溶液.则在此过程中,葡萄糖分子的下列哪种性质会发生改变( )
| A、分子的大小 |
| B、分子的总数目 |
| C、分子间的间隔 |
| D、分子中原子的数目 |
某探究小组设计了下列四种制备物质的实验方案,其中不能实现的是( )
| A、Fe2O3 稀H2SO4 Fe2(SO4)3溶液 NaOH 溶液 Fe(OH)3 |
| B、CuO 稀 HCl CuCl2溶液 Fe Cu |
| C、Fe 点燃 Fe2O3 稀H2SO4 Fe2(SO4)3溶液 |
| D、CaCO3 稀HCl CO2 NaOH溶液 Na2CO3溶液 |

