题目内容
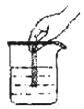
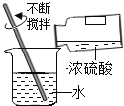
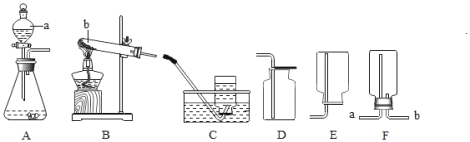
【题目】某同学可如图所示装置粗略的测定空气中氧气的体积分数。图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,其左端密封有空气和足量白磷(白磷着火点低,约40 ℃),右端跟空气相通,实验开始前,活塞处在5 cm处。
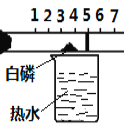
①可以观察到玻璃管内发生的现象:白磷(足量)__________,活塞先向(填左或右)______移动。
②恢复至常温,活塞应停在约___cm处,据此可得出的结论是______________。
【答案】发出白光,放出热量,产生大量白烟 右 4 空气中氧气约占空气体积的五分之一
【解析】
白磷在氧气中燃烧生成五氧化二磷。
①可以观察到玻璃管内发生的现象:白磷(足量)燃烧发出白光,放出热量,产生大量白烟,燃烧发出大量热,温度升高,玻璃管中压强增大,活塞先向右移动。
②空气中氧气约占空气体积的五分之一,恢复至常温,活塞应停在约4cm处,故可得出的结论是空气中氧气约占空气体积的五分之一。

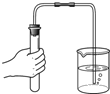
【题目】﹤1﹥根据如图所示的部分实验装置,回答有关问题
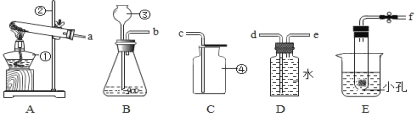
(1)写出图中仪器④的名称是_________。
(2)实验室常用装置A制O2,写出反应容器中产生O2 的化学方程式 _________ ;如用装置 D 进行收集,则应将导管 a 端与导管_____端相连。小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究。
(查阅资料):①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是____。
② K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
(猜想假设):假设I:只含KOH; 假设Ⅱ:含KOH和K2CO3; 假设Ⅲ:只含K2CO3
(进行实验):
实验操作步骤 | 实验现象 | 实验结论 |
① 取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设_____不正确 |
② 另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | ____ | 假设Ⅲ正确 |
③ 取②中上层清液,滴加无色酚酞溶液 | _____ |
(问题讨论):步骤②中加入过量BaCl2溶液的作用是________。
(拓展应用):完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是_________。