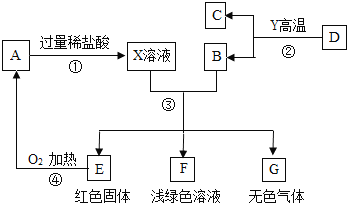
题目内容
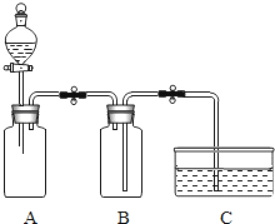
【题目】如图1是实验室制取气体的常用装置如图所示:
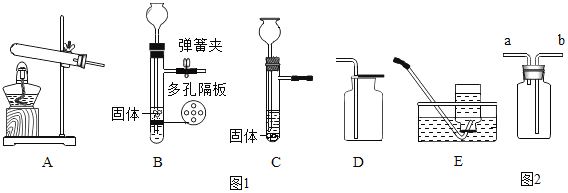
(1)实验室用KMnO4制取O2可选用A装置为发生装置;该反应的化学方程式为_____,该反应的基本类型为_____。
(2)实验室用来制取CO2的一套装置为_____(填字母代号),其中你所选择的发生装置的优点是_____。
(3)请简单写出实验室制取CO2的化学方程式_____;请写出实验室检验CO2化学方程式_____。
(4)若用如图2装置采用排水法收集O2,请简述操作步骤_____。
【答案】![]() ; 分解反应; BD; 可以控制反应的发生和停止;
; 分解反应; BD; 可以控制反应的发生和停止; ![]() ;
; ![]() ; 先把集气瓶装满水,然后氧气从a管进入
; 先把集气瓶装满水,然后氧气从a管进入
【解析】
(1)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平,属于分解反应;故答案为:![]() ;分解反应;
;分解反应;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;生成的二氧化碳可溶于水,密度比空气大,可用向上排空气法收集,所以实验室用来制取CO2的一套装置为BD,其中我所选择的发生装置的优点是:可以控制反应的发生和停止;故答案为:BD;可以控制反应的发生和停止;
(3)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:![]() ;
;![]() ;
;
(4)若用如图2装置采用排水法收集O2,先把集气瓶装满水,然后氧气从a管进入,因为氧气的密度比水小;故答案为:先把集气瓶装满水,然后氧气从a管进入;

【题目】某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应).已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O42H2O )的性质见下表:
熔点 | 沸点 | 热稳定性 | 其他 |
101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
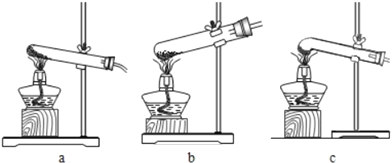
(1)下图是加热装置.最适宜的加热分解草酸晶体装置是 c.若选装置 a 可能会造成的后果是___;若选装置b可能会造成的后果是___.
(2)下图是验证热分解产物中含CO、CO2的装置.
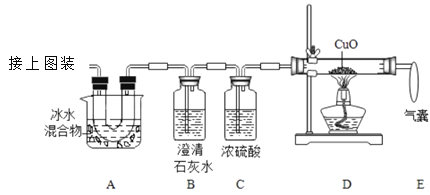
①装置A的作用是___,气囊的作用是___.
②证明存在CO2的现象是___,证明存在CO的现象是___.
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差.由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:___.
【题目】 某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2.这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
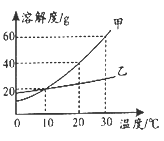
[查阅资料]通常状况下,1体积水约能溶解40体积SO2。
[实验方案]同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑料瓶变瘪,他们认为SO2与NaOH发生了反应。
[反思与改进]甲同学认为上述实验不够严谨,理由是_____。于是同学们设计了如下两个改进方案。
方案一
实验操作 | 实验现象 |
向两个充满SO2的200mL软塑料瓶中分别注入 10mL水和NaOH溶液,振荡,对比。 | 两个瓶子变瘪的程度完全相同 |
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是_____(填序号)。
a.15mL b.8mL c.5mL d.3mL
方案二
实验操作 | 实验现象 |
利用右图所示装置进行实验:
向两个充满SO2的300mL集气瓶中分别加入6mL水和NaOH溶液,一段时间后,打开止水夹,对比。 | 倒吸入两个集气瓶中的液体体积完全相同 |
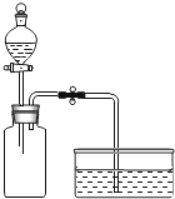
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是_____。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如图所示,你认为装置B的作用是_____。