题目内容
【题目】某化学兴趣小组欲进行粗盐的初步提纯实验。
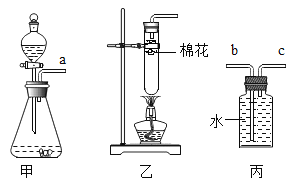
![]() 溶解过程中,用量筒量取一定体积的蒸馏水,读数时,视线与量筒内液体______保持相平。
溶解过程中,用量筒量取一定体积的蒸馏水,读数时,视线与量筒内液体______保持相平。
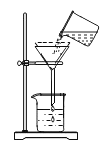
![]() 指出如图中过滤的错误之处
指出如图中过滤的错误之处
A______B______
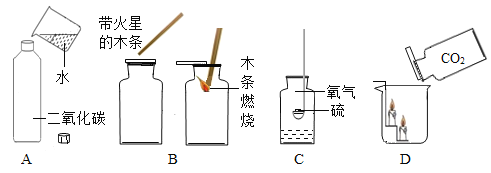
![]() 以下混合物能用溶解---过滤操作进行分离的是______
以下混合物能用溶解---过滤操作进行分离的是______
A 食盐和白糖 B 铁粉和铜粉 C 二氧化锰和氯化钾 D 豆油和水
![]() 蒸发操作中,除用到铁架台
蒸发操作中,除用到铁架台![]() 带铁圈
带铁圈![]() 酒精灯,玻璃棒,坩埚钳外,还需要用到______等仪器,该操作过程中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,你认为还可采用______
酒精灯,玻璃棒,坩埚钳外,还需要用到______等仪器,该操作过程中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,你认为还可采用______
![]() 粗盐提纯实验步骤包括:a过滤、b溶解、c蒸发、d称量精盐、e称量粗盐、f计算产率该实验步骤的正确顺序是______
粗盐提纯实验步骤包括:a过滤、b溶解、c蒸发、d称量精盐、e称量粗盐、f计算产率该实验步骤的正确顺序是______![]() 编号
编号![]() 其中,过滤,溶解,蒸发过程中都要用到的仪器是______,其作用分别是______,______,______。
其中,过滤,溶解,蒸发过程中都要用到的仪器是______,其作用分别是______,______,______。
![]() 最后得到的精盐属于______
最后得到的精盐属于______![]() 纯净物,混合物
纯净物,混合物![]()
![]() 已知:产率
已知:产率![]() 粗盐
粗盐![]() 精盐
精盐![]()
![]()
各小组的产率和评价如表:
组别 | 1 | 2 | 3 | 4 |
产率 | 90 | 80 | 70 | 92 |
评价 | 偏高 | 偏高 | 偏低 | 偏高 |
下面是各组同学对造成产率偏高偏低的原因的分析,你认为正确的是______
A 第1组,过滤时不小心捅破了滤纸
B 第2组,烧杯中的食盐水未溶解完就开始过滤
C 第3组,蒸发时搅拌不充分,液体溅出
D 第4组,没有蒸发干,精盐中含有水
【答案】凹液面的最低处 没用玻璃棒引流 漏斗的末端没有紧贴烧杯内壁 C 坩埚 来回移动酒精灯的方法 ebacdf 玻璃棒 加快粗盐的溶解 引流 使液体受热均匀,防止液体外溅 混合物 ACD
【解析】
(1)溶解过程中,用量筒量取一定体积的蒸馏水,读数时,视线与量筒内液体凹液面的最低处保持相平;故填:凹液面的最低处;
(2)如图中过滤的错误之处:A、没用玻璃棒引流;B、漏斗的末端没有紧贴烧杯内壁;故填:没用玻璃棒引流;漏斗的末端没有紧贴烧杯内壁;
(3)过滤适用于难溶于水的固体和能溶于水的固体的分离;
A、食盐和白糖均溶于水,不可用溶解-过滤的方法分离;
B、铁粉和铜粉均不溶于水,不可用溶解-过滤的方法分离;
C、二氧化锰难溶于水,氯化钾能溶于水,可用溶解-过滤的方法分离;
D、豆油和水均为液体,豆油不溶于水,不可用溶解-过滤的方法分离。
故填:C;
(4)蒸发操作中,除用到铁架台![]() 带铁圈
带铁圈![]() 酒精灯,玻璃棒,坩埚钳外,还需要用到坩埚等仪器,该操作过程中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采用来回移动酒精灯的方法,使坩埚均匀受热;故填:坩埚;来回移动酒精灯的方法;
酒精灯,玻璃棒,坩埚钳外,还需要用到坩埚等仪器,该操作过程中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采用来回移动酒精灯的方法,使坩埚均匀受热;故填:坩埚;来回移动酒精灯的方法;
(5)粗盐提纯实验步骤包括:e称量粗盐、b溶解、a过滤、c蒸发、d称量精盐、f计算产率,其中,过滤,溶解,蒸发过程中都要用到的仪器是玻璃棒,其作用分别是加快粗盐的溶解、引流、使液体受热均匀,防止液体外溅;故填:ebacdf;玻璃棒;加快粗盐的溶解;引流;使液体受热均匀,防止液体外溅;
(6)过滤只能除去不溶性的杂质,不能除去其它可溶性杂质,故得到的精盐是混合物;故填:混合物;
(7)A、过滤时不小心捅破了滤纸,使杂质混入了滤液中,致使精盐质量偏大,产率偏高,与评价相符;
B、烧杯中的食盐未溶解完就开始过滤,使精盐质量减小,产率偏低,与评价不符。
C、蒸发时搅拌不充分,液体溅出,使精盐质量减小,产率偏低,与评价相符;
D、没有蒸发干,精盐中含有水分,使精盐质量增大,产率偏高,与评价相符。;
故填:ACD。