题目内容
【题目】(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?若能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
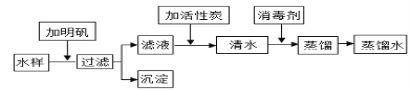
I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入3g氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
II.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量。 | 所得固体质量为①_________ |
III.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入②________g二氧化锰粉末,观察现象。 | D试管中产生气泡的速率更快 |
(实验结论)
(1)实验I、II证明:氧化铁可以作过氧化氢溶液分解的催化剂,请写出氧化铁催化过氧化氢分解的文字或符号表达式_____________。
(2)根据实验III的现象,你可以得到的结论____________。
(实验评价)
(3)经过讨论,同学认为实验结论(1)不严谨,要证明氧化铁可以作过氧化氢分解的催化剂,还需要补充一步实验,其操作为______________。
【答案】3g a 过氧化氢![]() 水+氧气 二氧化锰更适合做过氧化氢制氧气的催化剂 待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象;若试管中均产生大量气泡,带火星的木条均复燃,则证明[实验结论](1)成立
水+氧气 二氧化锰更适合做过氧化氢制氧气的催化剂 待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象;若试管中均产生大量气泡,带火星的木条均复燃,则证明[实验结论](1)成立
【解析】
[实验探究]实验I中A试管中产生气泡,带火星木条复燃,B试管中无明显现象证明产生的是氧气,氧化铁加快了过氧化氢的分解速率,试验Ⅱ中要证明氧化铁的可以作过氧化氢分解的催化剂,将实验I中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,其质量应该不变,所以所得固体质量为3g;
实验Ⅲ中根据对比试验中利用的控制变量法分析,变量是催化剂的种类,分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,则向D试管中也应加入ag二氧化锰粉末;
[实验结论](1)氧化铁催化过氧化氢分解生成水和氧气,化学反应表达式为:过氧化氢![]() 水+氧气;
水+氧气;
(2)根据实验Ⅲ的现象D试管中产生气泡的速率更快,所以二氧化锰更适合做过氧化氢制氧气的催化剂;故填:二氧化锰更适合做过氧化氢制氧气的催化剂;
[实验评价](3)根据催化剂的概念在化学反应中能够改变物质的反应速率,而其质量和化学性质在化学反应前后不变的物质叫催化剂,而实验探究Ⅰ没有证明氧化铁的化学性质,还需要补充一步实验,具有操作是待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象。若试管中均产生大量气泡,带火星的木条均复燃,则证明[实验结论](1)成立。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案【题目】同学们在学习了木炭还原氧化铜的实验后,联想到单质碳的一些化学性质,对反应后的气体成分产生了疑问,某学习小组对该反应产物中的气体成分进行了探究。
〔猜 想〕
①气体产物全部是CO2②气体产物全部是CO ③气体产物
〔查阅资料〕 CO气体能使湿润的黄色氯化钯试纸变蓝色。
〔设计实验〕根据各自的猜想,他们共同设计了如下图的实验装置进行探究。

〔现象与分析〕
现象 | 结论 |
如果装置B , 装置C无现象 | 则猜想①成立 |
如果装置B无现象,装置C | 则猜想②成立 |
如果装置B ,装置C____________ | 则猜想③成立 |
〔结论〕实验现象证明猜想③成立,同学们的疑问是合理的。
〔反思〕
(1)同学们对CO产生的原因进行了
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
②原因二:反应C+2CuO![]() 2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;
2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理______________________________________________。
(2)根据上述实验,请你归纳出单质碳在工业上的重要用途
【题目】化学使世界更美好,通过学习,我们有很多的收获。
收获一:世界万物都是由元素组成的,请用适当的化学符号填空:
(1)正三价的铝元素__________
(2)硝酸钾中的原子团__________
(3)人体中含量最多的物质___________
(4)植物光合作用的原料__________
(5)海水中除了水之外,含量最丰富的物质是___________
收获二:我们学会了从宏观和微观的角度认识物质世界。
(1)在水、铜和氦气三种物质中,__________(填化学式)是由原子直接构成;
(2)“![]() ”和“
”和“![]() ”表示不同元素的原子,以下图表示单质的是__________(选填编号);
”表示不同元素的原子,以下图表示单质的是__________(选填编号);

(3)食品中常加入防腐剂——苯甲酸钠(C6H5COONa)。该防腐剂由_______种元素组成,摩尔质量为____________,0.5mol的苯甲酸钠中约含有______________个氧原子
收获三:生活中处处有化学,“家”就是一个化学小世界,蕴含丰富的化学知识。
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指_________(选填“元素、原子、单质”)。
(2)下表为几种家用清洁剂的功能及有效成分:
名称 | 洁厕灵 | 活氧彩漂 | 漂白精 |
功能 | 有效清除污垢与异味 | 漂洗使衣物色彩鲜艳 | 快速漂除衣物污渍 |
有效成分 | HCl | H2O2 | NaClO |
Ⅰ.这些清洁剂属于__________(选填“混合物”或“纯净物”),若不小心把“洁厕灵”打翻在大理石地面上,会出现______________________的现象;
Ⅱ.![]() 中氢、氧元素质量比为___________
中氢、氧元素质量比为___________
Ⅲ.“洁厕灵”与“漂白精”不能混用,二者混合易产生一种有毒气体X。反应原理为:NaClO+2HCl→NaCl+X↑+H2O,则X的化学式为_________。
(3)玻璃中的主要成分![]() 属于______________(选填“金属氧化物”或“非金属氧化物”)
属于______________(选填“金属氧化物”或“非金属氧化物”)
(4)塑料诞生一百年来风光无限,它的发明者贝克兰也因此荣获“塑料之父”的美誉,而今由于人们使用不当而直接引发的一大环境问题是______________(填选编号)。
A.沙尘暴 B.水土流失 C.温室效应 D.白色污染
(5)天然气的主要成分是甲烷(CH4)一个甲烷分子的质量约为_______________克(只列式,不用计算结果)