题目内容
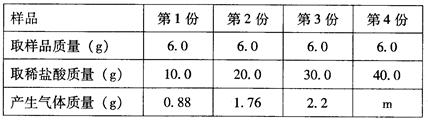
(6分)学校从某工厂购进一瓶赤铁矿样品(已被加工成粉末状,且其中杂质不含铁,也不与酸反应),其标签上的部分内容如下图所示,由于保存不当,标签部分信息丢失,为了解该样品中Fe2O3的质量分数,小明知道,铁锈的主要成分也是Fe2O3,他根据除锈的原理做了如下的探究活动:

(1)工业上用稀盐酸除锈的反应化学方程式为;
;
(2)为了测出样品中Fe2O3的含量,小明欲配制200g的7.3%的稀盐酸,则他需要40%浓盐酸的质量 ;
(3)在探究过程中小明测知10g的铁矿石样品,恰好与150g刚配好的稀盐酸完全反应,利用该组数据,求解10g该样品中Fe2O3质量(x)的比例为 ;
(4)根据该组数据小明也同样迅速计算出以下两组数据:
①铁矿石样品中Fe2O3的质量分数 ;
②若向反应后溶液中加入167g水,则最终所得溶液中溶质质量分数为 ;
(5)利用上述赤铁矿石冶炼56吨含铁97%的生铁,则需此矿石的质量 。

(1)工业上用稀盐酸除锈的反应化学方程式为;
;
(2)为了测出样品中Fe2O3的含量,小明欲配制200g的7.3%的稀盐酸,则他需要40%浓盐酸的质量 ;
(3)在探究过程中小明测知10g的铁矿石样品,恰好与150g刚配好的稀盐酸完全反应,利用该组数据,求解10g该样品中Fe2O3质量(x)的比例为 ;
(4)根据该组数据小明也同样迅速计算出以下两组数据:
①铁矿石样品中Fe2O3的质量分数 ;
②若向反应后溶液中加入167g水,则最终所得溶液中溶质质量分数为 ;
(5)利用上述赤铁矿石冶炼56吨含铁97%的生铁,则需此矿石的质量 。
(1)Fe2O3 +6HCl==2FeCl3 +3H2O;(2)36.5g; (3)160/219==X/(150g×7.3%)(或160/219==X/10.95g; (4)①80% ②5%; (5)97t
(1)略(2)考查的是溶液稀释的问题,溶液的稀释过程中加的是溶剂,故溶质不变,所以稀释前和稀释后的溶质质量相等,若假设浓盐酸的质量为X的话,即有200×7.3%=X·40%,所以X=36.5g
(3)解:设10g该样品中Fe2O3质量为X
Fe2O3 +6HCl==2FeCl3 +3H2O
160 219
X 150g×7.3%
∴160/219==X/(150g×7.3%)
(4) ①由上解可求得X=8,故铁矿石样品中Fe2O3的质量分数为8g/10g×100%=80%
②由于10g的铁矿石样品,恰好与150g刚配好的稀盐酸完全反应,且其中杂质不含铁,也不与酸反应,所以反应后的溶质为FeCl3,设其质量为y,
Fe2O3 +6HCl==2FeCl3 +3H2O
219 325
150g×7.3% y
∴219/325="=" (150g×7.3%) /y
y=16.25g
又∵由于在此反应中无气体和沉淀生成,且杂质不与酸反应,所以反应后的溶液质量为150g+8g=158g,再加167g水,溶液总质量为325g,∴最终所得溶液中溶质质量分数为16.25g/325g×100%=5%
(5)此题考查的是在化学变化中,元素的质量守恒,即元素质量不变,也就是赤铁矿石中含有的铁元素质量和生铁中含有的铁元素质量相等。
设需此矿石的质量为x吨,则有x·80%×70%=56×97%,(其中70%为Fe2O3中Fe的质量分数),x=97
(3)解:设10g该样品中Fe2O3质量为X
Fe2O3 +6HCl==2FeCl3 +3H2O
160 219
X 150g×7.3%
∴160/219==X/(150g×7.3%)
(4) ①由上解可求得X=8,故铁矿石样品中Fe2O3的质量分数为8g/10g×100%=80%
②由于10g的铁矿石样品,恰好与150g刚配好的稀盐酸完全反应,且其中杂质不含铁,也不与酸反应,所以反应后的溶质为FeCl3,设其质量为y,
Fe2O3 +6HCl==2FeCl3 +3H2O
219 325
150g×7.3% y
∴219/325="=" (150g×7.3%) /y
y=16.25g
又∵由于在此反应中无气体和沉淀生成,且杂质不与酸反应,所以反应后的溶液质量为150g+8g=158g,再加167g水,溶液总质量为325g,∴最终所得溶液中溶质质量分数为16.25g/325g×100%=5%
(5)此题考查的是在化学变化中,元素的质量守恒,即元素质量不变,也就是赤铁矿石中含有的铁元素质量和生铁中含有的铁元素质量相等。
设需此矿石的质量为x吨,则有x·80%×70%=56×97%,(其中70%为Fe2O3中Fe的质量分数),x=97

练习册系列答案
相关题目

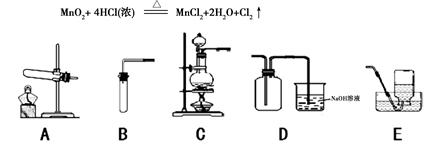
 2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?
2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?