题目内容
请从C,H,O,S,Cl,Na,Fe等7种元素中选择恰当的元素,用离子符号、化学式或化学方程式按下列要求填空:
(1)硫酸钠中的阴离子 ;氯化铁中的阳离子 ;由四种元素组成的盐(只写一种) .
(2)写出一个置换反应的化学方程式: ;写出一个有气体生成的复分解反应的化学方程式: .
(1)硫酸钠中的阴离子 ;氯化铁中的阳离子 ;由四种元素组成的盐(只写一种) .
(2)写出一个置换反应的化学方程式: ;写出一个有气体生成的复分解反应的化学方程式: .
SO42﹣;Fe3+; NaHCO3; Fe+H2SO4═FeSO4+H2↑ ; Na2CO3+2HCl═2NaCl+H2O+CO2↑
试题分析: (1)硫酸钠由钠离子阳离子和硫酸根离子阴离子构成;氯化铁由铁离子阳离子和氯离子阴离子构成;盐中含有金属阳离子和酸根阴离子,含有四种元素,常见的为碳酸氢钠;(2)依据置换反应的特点,用活泼金属铁与常见的酸盐酸或稀硫酸均可;常见有气体生成的复分解反应为酸与碳酸盐,用盐酸或稀硫酸与碳酸钠或者碳酸氢钠均可。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
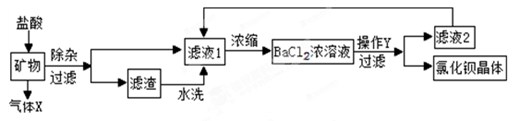
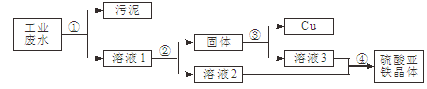
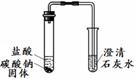
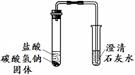
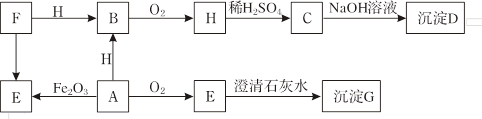
 E的化学方程式 ;
E的化学方程式 ;