题目内容
【题目】A、B、C、D、E、F各表示化合物的化学式,根据下列反应:
A+B→C+H2O C+NaOH→D(蓝色)↓+E
D→A+H2O E+BaCl2→F(白色)↓+2NaCl
回答下列问题:
(1)写出下列化学式:A , B , D , F
(2)写出化学方程式D→A+H2O: .
【答案】
(1)CuO;H2SO4;Cu(OH)2;BaSO4
(2)Cu(OH)2 ![]() CuO+H2O
CuO+H2O
【解析】解:根据D是蓝色沉淀,可知D是氢氧化铜,C是含有铜离子的盐,E是含有钾离子的盐,B和D反应生成C和水,所以B是酸,E能和氯化钡溶液反应白色,不溶于稀硝酸的沉淀F,可知F是硫酸钡,那么E就是硫酸钾,C是硫酸铜,B是硫酸,A和硫酸反应生成硫酸铜和水,可知A是氧化铜,通过验证,推断结果符合题意.
所以(1)推断有关物质的化学式:A为CuO,B为H2SO4 , D为Cu(OH)2 , F为BaSO4;(2)D→A+H2O,即氢氧化铜加热生成铜和水,故反应的方程式为Cu(OH)2 ![]() CuO+H2O.
CuO+H2O.
所以答案是:(1)CuO,H2SO4 , Cu(OH)2 , BaSO4;(2)Cu(OH)2 ![]() CuO+H2O.
CuO+H2O.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

【题目】含有铵根离子的物质称为农业生产中的铵态氮肥,如表是氮肥氧化铵不同温度下的溶解度:
温度℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
(1)从表中可知:在70℃时,50g水中最多溶解氯化铵克.
(2)烧杯A是70℃时,含有100g水的氯化铵不饱和溶液,经过如图的变化过程(在整个过程中不考虑水分的蒸发),则到C烧杯时,溶液的质量为g.
(3)如图所示,是对氯化铵性质的探究实验: 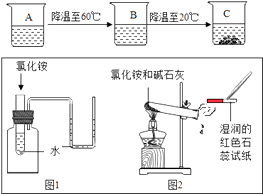
①图1说明氯化铵溶液水会热量;
②图2是观察到湿润红色石蕊试纸变色;
③农业生产中(填“能”或“不能”)将铵态氮肥与碱性物质混用.