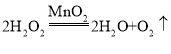题目内容
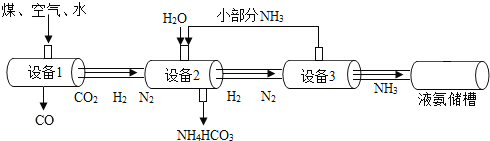
【题目】某化肥厂以煤、空气、水为原料合成氨,生产流程如图:
(1)NH3 中氮元素的化合价为_____。
(2)设备 2 中参加反应的物质有_____。
(3)设备 3 中发生反应的化学方程式为_____________。
(4)NH4HCO3 中氮元素的质量分数为_________。
【答案】-3 NH3、H2O、CO2 3H2+N2 2NH3 17.7%
2NH3 17.7%
【解析】
(1)在氨气中,氢元素显示+1价,根据化合物中元素化合价代数和为0,所以氮元素的化合价为-3价;
(2)由生产流程图可知,设备2中参加反应的物质有NH3、H2O、CO2;
(3)设备 3 中氢气和氮气反应生成氨气,方程式还是:3H2+N2 2NH3;
2NH3;
(4)在NH4HCO3中氮元素的质量分数为:![]() ×100%≈17.7%。
×100%≈17.7%。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
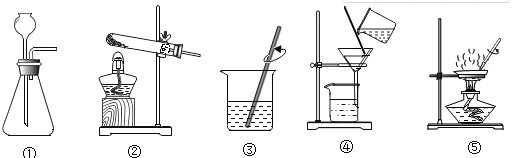
(1)实验室用高锰酸钾制取氧气时,选用的发生装置是________(填数字序号),反应的化学方程式为_________。 (2)溶解NaCl时,③中玻璃棒的作用是 ___________。 | (1)实验室制取二氧化碳时,选用的发生装置是________(填数字序号),反应的化学方程式为_________。 (2)粗盐提纯时,⑤中玻璃棒的作用是___________。 |
可供选择的实验或操作:
| |
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、 CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:
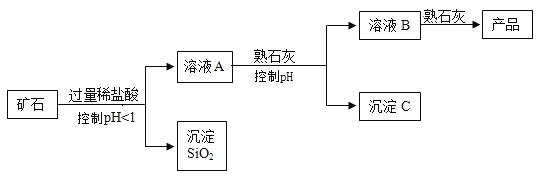
部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)溶液A中的阳离子有________________种。溶液A与熟石灰反应控制PH范围为_______________。
(2)沉淀C的成分是________________。
(3)溶液B与熟石灰反应的化学方程式是______________。该反应类型为_______________反应。
(4)从理论上讲,矿石中镁元素质量与产品中镁元素质量是否相等? _______________(填“是”或“否”)。