题目内容
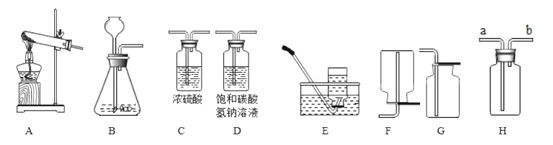
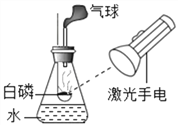
【题目】CO2在高温下能与木炭反应生成CO。为验证该反应,某课外兴趣小组设计了一套实验装置,装置图如下:
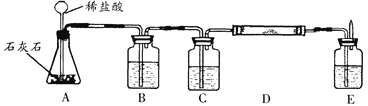
(1)根据装置图,填写下表:
仪器标号 | 仪器中所加物质 | 作用 |
A | 石灰石,稀盐酸 | 石灰石与盐酸作用产生CO2 |
B | 饱和碳酸氢钠溶液(与CO2不反应) | 除去CO2中的HCl气体 |
C | _____________________ | ____________ |
D | __________________ | ________________ |
E | ______________ | ________________ |
(2)D处要增加的仪器的名称是___________________________。
【答案】 浓硫酸 除去CO2中的水蒸气 木炭粉 与CO2在高温下反应 NaOH溶液(或澄清石灰水) 吸收(除去)CO2 酒精灯或酒精喷灯
【解析】(1)C中装有浓硫酸,浓硫酸有吸水性,故其作用是吸水作干燥剂;D中装有木炭,作用是在高温下和二氧化碳反应生成一氧化碳;E中装有NaOH溶液,作用是吸收未反应的CO2;
(2)根据碳与二氧化碳反应需要高温分析解答。(1)C中装有浓硫酸,浓硫酸有吸水性,故其作用是除去CO2中的水蒸气 ;D中装有木炭粉,作用是与CO2在高温下反应;E中装有NaOH溶液(或澄清石灰水),作用是吸收(除去)CO2;(2)碳与二氧化碳反应需要高温,D处要增加的仪器的名称是酒精灯或酒精喷灯。

【题目】碱石灰是CaO和NaOH固体的混合物,常用作干燥剂。碱石灰在空气中久置会吸收空气中的水和二氧化碳而变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。请你参与探究过程:

【查阅资料】①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性。
(1)在操作一实验过程中,同学们发现向样品中加水时放出大量的热。据此实验,下列对样品成分分析正确的是________(填序号)。
A. 一定有NaOH B. 一定有Na2CO3 C. 一定有CaO D. 至少有NaOH、CaO中的一种
(2)在操作二之后所得的固体A中一定含有________。
(3)实验小组的同学继续对溶液B中的溶质进行了探究。
【猜想假设】猜想一:NaOH 猜想二:Na2CO3
猜想三:NaOH和Na2CO3 猜想四:Ca(OH)2和________
【实验验证】为进一步确认溶液B中溶质的成分,做了如下实验。
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,用pH试纸检测滤液的pH | ①__________________; ②pH>7 | 猜想三正确 |
实验步骤①中发生的化学反应方程式是________________________________,其实验目的是________________________________。
【反思评价】对于像碱石灰这样容易变质的物质,保存时需要注意密封保存。