题目内容
【题目】下列做法正确的是( )
A.氢氧化钠溶液沾到皮肤上,要立即涂上硼酸溶液
B.图书、档案着火,用干粉灭火器
C.生活中用煮沸的方法将硬水软化
D.用钢丝刷除去铝制品表面的氧化物
【答案】C
【解析】
A、氢氧化钠溶液沾到皮肤上,立即用大量水冲洗,再涂上硼酸溶液,故选项说法错误。
B、二氧化碳灭火后不留有痕迹,不会造成图书档案的损坏,可以用来扑灭图书、档案等火灾,图书、档案着火,应用二氧化碳灭火器,故选项说法错误。
C、煮沸能降低水中可溶性钙镁化合物的含量,生活中用煮沸的方法将硬水软化,故选项说法正确。
D、铝制品表面有一层致密的氧化铝薄膜,用钢丝球擦洗,会破坏氧化铝薄膜,不能用钢丝球擦洗,故选项说法错误。
故选:C。

【题目】为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的速率影响效果,某研究小组进行了如下探究: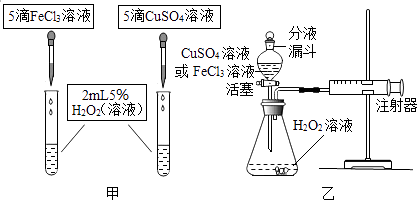
【定性研究】
(1)如图甲,可通过观察来定性比较两者的速率影响效果.
(2)【定量研究】
如图乙,实验前检查该装置气密性的方法是 . 要定量比较两者的速率影响效果,可测量生成等体积气体所需的 .
(3)【深入研究】
在FeCl3溶液中,究竟是哪种粒子影响过氧化氢的分解速率?
猜想1:水分子(H2O)影响过氧化氢的分解速率;
猜想2:影响过氧化氢的分解速率;
猜想3:影响过氧化氢的分解速率;…
请设计实验,验证猜想
实验操作 | 实验现象 | 实验结论 |
分别取同温度同体积同浓度的H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl.观察现象. | 加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢. | 证明是Fe3+影响过氧化氢的分解速率 |
(4)【反思与讨论】上述实验确实可以证明Fe3+可以改变过氧化氢的分解速率,但不能证明FeCl3是过氧化氢分解的催化剂.若要证明FeCl3是过氧化氢分解的催化剂,还需要通过实验证明FeCl3在反应前后 .
请写出FeCl3催化H2O2分解的化学方程式 .
