题目内容
【题目】小明学习了“氧气的实验室制法”后,对二氧化锰的催化作用产生了浓厚兴趣。如何从高锰酸钾制取氧气后的固体残留物中提纯二氧化锰?小明和同学们做了如下探究。
(提出问题)如何从高锰酸钾制取氧气后的固体残留物中提纯二氧化锰?
(查阅资料)
(1)二氧化锰是黑色无定形粉末,或黑色斜方晶体。难溶于水、弱酸、弱碱、硝酸、冷硫酸。
(2)锰酸钾![]() 化学式:
化学式:![]() 呈墨绿色或灰黑色正交晶体,
呈墨绿色或灰黑色正交晶体,![]() 时分解,溶于水、氢氧化钠和氢氧化钾水溶液,其水溶液呈墨绿色或深绿色。
时分解,溶于水、氢氧化钠和氢氧化钾水溶液,其水溶液呈墨绿色或深绿色。
(实验步骤)
(1)取适量的高锰酸钾于大试管中,加热至不再产生气体为止,其目的是__,反应的符号表达式是__。
(2)待试管冷却后,将试管中的固体置于烧杯中,加入足量的水,并用玻璃棒不断搅拌,是为了___。
(3)将装有混合物的烧杯放于实验台上,静置一段时间后,可观察到上层清液呈_____色。
(4)过滤,该操作中所用到的玻璃仪器是_______;洗涤,目的是_______;干燥。
(5)取![]() 得到的固体适量于试管中,加入少量的过氧化氢溶液,可观察到_______。
得到的固体适量于试管中,加入少量的过氧化氢溶液,可观察到_______。
(反思)由上述步骤可知,实验前后二氧化锰的_______没有改变。
【答案】为了分解高锰酸钾,制得锰酸钾和二氧化锰的混合物 KMnO4![]() K2MnO4+MnO2+O2 为了使混合物中的锰酸钾溶于水 墨绿色或深绿色 漏斗,烧杯、玻璃棒 除去二氧化锰固体表面的残留液体 大量的气泡冒出 化学性质不变
K2MnO4+MnO2+O2 为了使混合物中的锰酸钾溶于水 墨绿色或深绿色 漏斗,烧杯、玻璃棒 除去二氧化锰固体表面的残留液体 大量的气泡冒出 化学性质不变
【解析】
(1)取适量的高锰酸钾于大试管中,加热至不再产生气体为止,其目的是为了分解高锰酸钾,制得锰酸钾和二氧化锰的混合物。高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,反应的符号表达式为:KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2
(2)混合固体中的锰酸钾易溶于水,而二氧化锰不溶于水,故该步骤的目的是为了使混合物中的锰酸钾溶于水。
(3)锰酸钾的水溶液呈墨绿色或深绿色。
(4)过滤操作中用到的玻璃仪器有漏斗,烧杯、玻璃棒。过滤后洗涤步骤可以除去二氧化锰固体表面的残留液体。
(5)二氧化锰与过氧化氢反应生成大量的氧气,故实验现象是有大量的气泡冒出。从而说明二氧化锰在反应前后的化学性质没有变。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
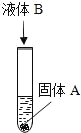
学业测评一课一测系列答案【题目】如图所示,试管中盛有固体物质 A,向试管中加入一种液体物质 B 后,观察 到有气泡产生.请你依据上述实验现象,对 A和 B 的组合至少做出三种猜想(要求三种组合中 的固体 A 分别属于不同类别的物质):
A | B | |
猜想 1 | ____ | ____ |
猜想 2 | ____ | ____ |
猜想 3 | ____ | ____ |
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:(1)m的值为_____g
(2)该石灰石样品的纯度._____。
(3)反应完全后最终溶液中氯化钙的质量分数?_____。