题目内容
某校化学研究性学习小组进行铝与稀硫酸、稀盐酸反应的实验.
(1)实验发现,铝与稀硫酸、稀盐酸都能发生反应生成氢气,原因是
(2)分别写出铝与稀硫酸、稀盐酸反应的化学方程式
(3)【发现问题】
用擦去氧化膜的相同大小的铝片分别与H+浓度相同的稀硫酸和稀盐酸反应时,实验现象明显不同:铝与稀硫酸反应产生气泡比铝与稀盐酸反应产生气泡慢得多.
【假设】
①甲同学认为:硫酸电离产生的SO42-对反应有抑制作用.
②乙同学认为:盐酸电离产生的Cl-对反应有促进作用.
【设计实验并验证】
为了验证甲、乙两位同学的观点,丙、丁两位同学分别设计了实验方案1(验证甲同学的观点)和实验方案2(验证乙同学的观点).
请你在下表中相应空格填空:
(4)【实验拓展】
用擦去氧化膜的铝片与稀硝酸反应,发现也有气泡产生,但经检验该气体不是氢气.请你分析出现这种情况的可能原因
(1)实验发现,铝与稀硫酸、稀盐酸都能发生反应生成氢气,原因是
铝排在氢的前面,能与酸反应置换反应生成氢气.
铝排在氢的前面,能与酸反应置换反应生成氢气.
.(2)分别写出铝与稀硫酸、稀盐酸反应的化学方程式
2Al+3H2SO4 ═Al2(SO4)3+3H2↑
2Al+3H2SO4 ═Al2(SO4)3+3H2↑
、2Al+6HCl═2AlCl3+3H2↑
2Al+6HCl═2AlCl3+3H2↑
.(3)【发现问题】
用擦去氧化膜的相同大小的铝片分别与H+浓度相同的稀硫酸和稀盐酸反应时,实验现象明显不同:铝与稀硫酸反应产生气泡比铝与稀盐酸反应产生气泡慢得多.
【假设】
①甲同学认为:硫酸电离产生的SO42-对反应有抑制作用.
②乙同学认为:盐酸电离产生的Cl-对反应有促进作用.
【设计实验并验证】
为了验证甲、乙两位同学的观点,丙、丁两位同学分别设计了实验方案1(验证甲同学的观点)和实验方案2(验证乙同学的观点).
请你在下表中相应空格填空:
| 实验操作 | 实验现象 | 实验结论 | |
| 方案1 | 甲同学观点错误 | ||
| 方案2 | 乙同学观点正确 |
用擦去氧化膜的铝片与稀硝酸反应,发现也有气泡产生,但经检验该气体不是氢气.请你分析出现这种情况的可能原因
硝酸具有强氧化性,与金属反应不产生氢气.
硝酸具有强氧化性,与金属反应不产生氢气.
.分析:(1)根据铝的金属活动性分析
(2)根据金属与酸反应的规律写出方程式
(3)从微观角度分析得出,H+浓度相同的盐酸、硫酸中,只是所含酸根离子不同.从酸根离子考虑设计实验方案.
(4)根据硝酸的强氧化性分析
(2)根据金属与酸反应的规律写出方程式
(3)从微观角度分析得出,H+浓度相同的盐酸、硫酸中,只是所含酸根离子不同.从酸根离子考虑设计实验方案.
(4)根据硝酸的强氧化性分析
解答:解:(1)铝排在氢的前面,能与酸反应置换反应生成氢气,因此铝能与盐酸和硫酸都反应产生氢气;
(2)铝与硫酸反应生成硫酸铝和氢气,铝与盐酸反应产生氯化铝和氢气,反应的化学方程式分别为
2Al+3H2SO4 ═Al2(SO4)3+3H2↑;2Al+6HCl═2AlCl3+3H2↑
(3)反应条件中铝片的大小、外形均相同,H+浓度相同的稀盐酸、稀硫酸反应,只有酸根离子不同,考虑酸根离子对反应速率的影响设计实验方案.
甲同学:硫酸根离子对铝与酸的反应有抑制作用.为了验证该假设,在铝与硫酸反应的溶液中加入硫酸钠固体,观察反应速率.甲同学观点错误,说明反应速率不变
乙同学:氯离子对铝与酸的反应有促进作用.为了验证该假设,在铝与硫酸反应的溶液中加入氯化钠固体,观察反应速率是否加快.乙同学观点正确,说明反应速率加快了,证明氯离子对铝与酸的反应有促进作用
(4)硝酸具有氧化性,与金属反应不产生氢气.
故答案为:(1)铝排在氢的前面,能与酸反应置换反应生成氢气..
(2)2Al+3H2SO4 ═Al2(SO4)3+3H2↑
、2Al+6HCl═2AlCl3+3H2↑
.
(3)
(4)硝酸具有强氧化性,与金属反应不产生氢气.
(2)铝与硫酸反应生成硫酸铝和氢气,铝与盐酸反应产生氯化铝和氢气,反应的化学方程式分别为
2Al+3H2SO4 ═Al2(SO4)3+3H2↑;2Al+6HCl═2AlCl3+3H2↑
(3)反应条件中铝片的大小、外形均相同,H+浓度相同的稀盐酸、稀硫酸反应,只有酸根离子不同,考虑酸根离子对反应速率的影响设计实验方案.
甲同学:硫酸根离子对铝与酸的反应有抑制作用.为了验证该假设,在铝与硫酸反应的溶液中加入硫酸钠固体,观察反应速率.甲同学观点错误,说明反应速率不变
乙同学:氯离子对铝与酸的反应有促进作用.为了验证该假设,在铝与硫酸反应的溶液中加入氯化钠固体,观察反应速率是否加快.乙同学观点正确,说明反应速率加快了,证明氯离子对铝与酸的反应有促进作用
(4)硝酸具有氧化性,与金属反应不产生氢气.
故答案为:(1)铝排在氢的前面,能与酸反应置换反应生成氢气..
(2)2Al+3H2SO4 ═Al2(SO4)3+3H2↑
、2Al+6HCl═2AlCl3+3H2↑
.
(3)
| 在铝与硫酸反应的溶液中加入硫酸钠固体 | 反应速度不变 | ||
| 在铝与硫酸反应的溶液中加入氯化钠固体, | 反应速度加快 |
点评:本题在考查“影响反应速率的因素”这个知识点时,采用了多个不同的例子,通过对比实验,得到结果分析生成结论,注重考查学生的分析问题和解决问题的能力.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的探究过程如下:
[提出问题]样品中碳酸钠的质量分数是多少?
[知识准备]
食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠;反应过程中不考虑水和氯化氢的挥发.
[设计方案并实验]
甲组同学:称取12.00样品,加水配成溶液,在溶液中加入过量澄清石灰水,过滤、洗涤、干燥,共得到白色沉淀10.00g.
乙组同学:称取12.00样品,加入足量的稀盐酸直到反应停止,共收集到4.4g二氧化碳.
[解决问题]
请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量是 ,碳酸钠的质量分数是 .(计算结果精确到0.1%)
[交流反思]
(1)甲组的小青同学认为,要求出碳酸钠的质量,也可以使用与盐酸和石灰水所属类别不同的其他物质 (填一种具体物质的化学式)的溶液与样品反应,通过测定相关物质的质量,进行有关计算即可.
(2)乙组的小雨同学认为,所用稀盐酸的溶质质量分数也可求出:取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
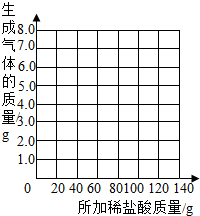
表中数据a= g,b= g.并请你在下边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.
[提出问题]样品中碳酸钠的质量分数是多少?
[知识准备]
食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠;反应过程中不考虑水和氯化氢的挥发.
[设计方案并实验]
甲组同学:称取12.00样品,加水配成溶液,在溶液中加入过量澄清石灰水,过滤、洗涤、干燥,共得到白色沉淀10.00g.
乙组同学:称取12.00样品,加入足量的稀盐酸直到反应停止,共收集到4.4g二氧化碳.
[解决问题]
请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量是
[交流反思]
(1)甲组的小青同学认为,要求出碳酸钠的质量,也可以使用与盐酸和石灰水所属类别不同的其他物质
(2)乙组的小雨同学认为,所用稀盐酸的溶质质量分数也可求出:取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
| 加入盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.9 | 97.8 | 116.7 | 135.60 | 155.05 | 175.05 | 195.05 |
| 生成气体的质量/g | 1.1 | 2.2 | a | 4.4 | 4.95 | b | -- |

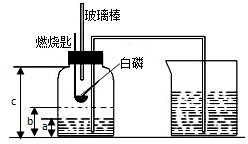 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: