题目内容
在反应4X+2Y=N+3M中,已知N和M的相对分子质量之比为22:9,当1.7gX与Y完全反应后,生成6.6g的N,则在此反应中Y和N的质量比是( )
| A、65:33 | B、16:9 |
| C、32:9 | D、46:9 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:①根据化学方程式和已知条件“N和M的相对分子质量之比为22:9”以及N的质量,列出比例式,即可求出M的质量;
②根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则参加的Y的质量=N的质量+M的质量-X的质量;然后写出两者的比,据此选择即可.
②根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则参加的Y的质量=N的质量+M的质量-X的质量;然后写出两者的比,据此选择即可.
解答:解:①应为根据已知条件“N和M的相对分子质量之比为22:9”,则N:3M=22:3×9=22:27,
设生成的M的质量为a,
∴22:27=6.6g:a
解之得:a=8.1g;
②根据质量守恒定律可得Y的质量=6.6g+8.1g-1.7g=13g;
∴此反应中Y和N的质量比是13g:6.6g=65:33.
故选A.
设生成的M的质量为a,
∴22:27=6.6g:a
解之得:a=8.1g;
②根据质量守恒定律可得Y的质量=6.6g+8.1g-1.7g=13g;
∴此反应中Y和N的质量比是13g:6.6g=65:33.
故选A.
点评:本题和我们平时所做的根据化学方程式的计算正好相反,解本题的关键是掌握根据化学方程式计算的原理.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列图示的实验操作中,正确的是( )
A、 |
B、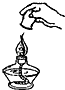 |
C、 |
D、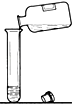 |
下列物质中,既有可燃性,又有还原性的气体是( )
| A、氢气 | B、氧气 | C、木炭 | D、水蒸气 |
当前食品安全备受人们关注.下列做法会严重威胁人体健康的是( )
| A、长期饮用白开水 |
| B、蒸馒头加适量小苏打 |
| C、用甲醛保鲜白菜 |
| D、食品袋里充入氮气延长食品的保质期 |
下列实验基本操作正确的是( )
A、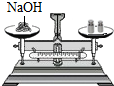 称量NaOH固体 |
B、 液体的量取 |
C、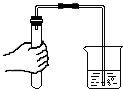 检查装置气密性 |
D、 加热液体 |
以下是一些常用的危险品标志,装运酒精的包装箱应贴的标志是( )
A、 |
B、 |
C、 |
D、 |
下列实验操作或记录正确的是( )
| A、用10mL量筒量取了8.65mL的水 |
| B、用托盘天平称量5.65g氯化钠 |
| C、使用托盘天平称量时,用镊子取放砝码 |
| D、实验时未经洗净的滴管可直接再吸取别的试剂 |