题目内容
【题目】实验是学习化学的一条重要途径,请结合所学知识,根据下图回答问题。
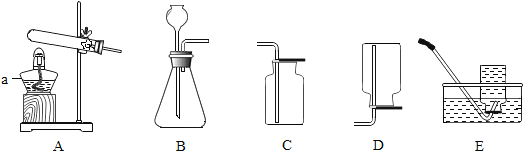
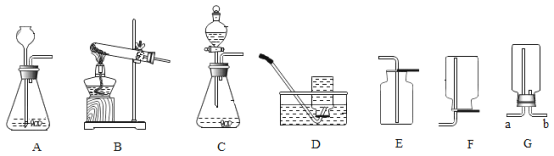
(1)仪器a的名称为_____;
(2)实验室用高锰酸钾制取氧气时,试管口向下倾斜的目的是_____;反应的化学符号表达式为_____;
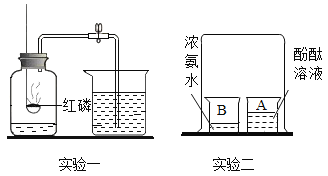
(3)氧气的化学性质比较活泼,很多物质能与氧气反应,请写出细铁丝在氧气中反应的符号表达式_____;磷与氧气反应的符号表达式_____,实验室利用该反应可以测定空气中氧气的含量,在该实验中(选“能”或“否”)_____将红磷换成细铁丝,理由_____;
(4)实验室用过氧化氢制氧气时,选用的发生装置中的长颈漏斗还可改为分液漏斗,即可控制反应的_____;要收集较纯净的氧气选用的收集装置是_____(填字母序号),收集时要等到_____才开始收集;该反应的化学符号表达式为_____;
(5)已知实验室可用固体石灰石和盐酸溶液在常温下反应制取二氧化碳气体,二氧化碳的密度比空气大,且能溶于水,请从上图中选择实验室制取二氧化碳的发生装置_____;收集装置_____;
【答案】酒精灯 防止冷凝水倒流进试管底部引起试管炸裂 KMnO4![]() K2MnO4+MnO2+O2 Fe + O2
K2MnO4+MnO2+O2 Fe + O2 ![]() Fe3O4 P + O2
Fe3O4 P + O2 ![]() P2O5 否 铁在空气中不能燃烧 速率 E 气泡连续均匀冒出 H2O2
P2O5 否 铁在空气中不能燃烧 速率 E 气泡连续均匀冒出 H2O2![]() H2O+O2 B C
H2O+O2 B C
【解析】
(1)仪器a的名称为酒精灯;
(2)实验室用高锰酸钾制取氧气时,试管口向下倾斜的目的是防止冷凝水倒流进试管底部引起试管炸裂;高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的符号表达式为: KMnO4![]() K2MnO4+MnO2+O2;
K2MnO4+MnO2+O2;
(3)细铁丝在氧气中燃烧生成四氧化三铁,反应的符号表达式为:Fe + O2 ![]() Fe3O4;磷与氧气反应生成五氧化二磷,反应的符号表达式为:P + O2
Fe3O4;磷与氧气反应生成五氧化二磷,反应的符号表达式为:P + O2 ![]() P2O5;实验室利用该反应可以测定空气中氧气的含量,在该实验中不能将红磷换成细铁丝,因为铁在空气中不能燃烧;(4)分液漏斗能控制液体的滴加速率,从而控制反应的速率。实验室用过氧化氢制氧气时,选用的发生装置中的长颈漏斗还可改为分液漏斗,即可控制反应的速率;氧气的不易溶于水,密度大于空气,可用排水法和向上排空气法收集,排水法收集的气体较纯,要收集较纯净的氧气选用的收集装置是E;收集时要等到气泡连续均匀冒出时才开始收集;过氧化氢在二氧化锰催化作用下分解生成水和氧气,该反应的化学符号表达式为H2O2
P2O5;实验室利用该反应可以测定空气中氧气的含量,在该实验中不能将红磷换成细铁丝,因为铁在空气中不能燃烧;(4)分液漏斗能控制液体的滴加速率,从而控制反应的速率。实验室用过氧化氢制氧气时,选用的发生装置中的长颈漏斗还可改为分液漏斗,即可控制反应的速率;氧气的不易溶于水,密度大于空气,可用排水法和向上排空气法收集,排水法收集的气体较纯,要收集较纯净的氧气选用的收集装置是E;收集时要等到气泡连续均匀冒出时才开始收集;过氧化氢在二氧化锰催化作用下分解生成水和氧气,该反应的化学符号表达式为H2O2![]() H2O+O2;
H2O+O2;
(5)实验室可用固体石灰石和盐酸溶液在常温下反应制取二氧化碳气体,是固体和液体,在常温下的反应,故选用发生装置B;二氧化碳的密度比空气大,且能溶于水,故选用的是收集装置是C。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,化学兴趣小组据此设计了如下探究方案。
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验试剂)5%的过氧化氢溶液、红砖粉末、二氧化锰粉末
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释 |
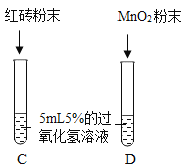
步骤1: ____________________________ | A试管中无明显现象 B试管中产生大量能使带火星木条复燃的气体 | ①产生的气体是_________ ②红砖粉末能改变过氧化氢的分解速率 |
步骤2 向B试管中重新加入5% 的过氧化氢溶液,反应停止后 过滤、洗涤、干燥、称量滤渣 | ③B试管中又产生大量能使带火星木条复燃的气体 ④滤渣质量维持不变 | ⑤红砖粉末的__________和____________不变,能作过氧化氢分解的催化剂 |
步骤3: 为了保证图中对比实验具 有可比性,两种粉末的质量应 ________________________ | ⑥两试管中均产生气泡且 ______________________ | 红砖粉末的催化效果没有二氧化锰粉末好。 ⑦写出红砖粉末催化过氧化 氢分解的化学方程式 ______________________ |