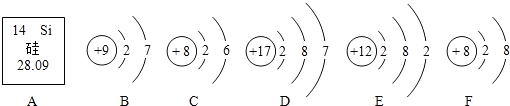题目内容
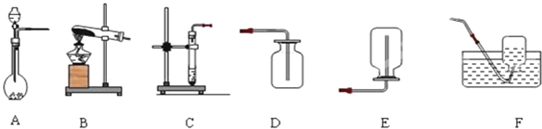
根据如图回答问题.
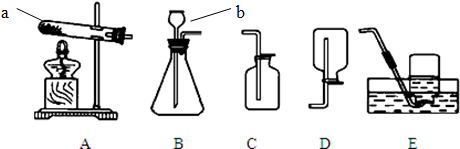
(1)请写出下列仪器的名称:a ;b .
(2)实验室制取二氧化碳反应的化学方程式是 ,所选用的发生装置是 .(填对应装置序号,下同)
(3)实验室用高锰酸钾制取氧气反应的化学方程式是 ,所选用的收集装置是E或 .主要的实验步骤有:①加热;②装药品并固定试管;③检查装置气密性;④用排水法收集氧气;⑤停止加热;⑥将导管从水槽中取出.正确的操作顺序是 .
(4)工业上分离液态空气的方法制取氧气,主要是利用了氧气和氮气的 不同.
(5)实验室需要制备16g氧气,则理论上需要分解H2O2的质量为 g.

(1)请写出下列仪器的名称:a
(2)实验室制取二氧化碳反应的化学方程式是
(3)实验室用高锰酸钾制取氧气反应的化学方程式是
(4)工业上分离液态空气的方法制取氧气,主要是利用了氧气和氮气的
(5)实验室需要制备16g氧气,则理论上需要分解H2O2的质量为
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)高锰酸钾受热时容易扩散,分解能生成锰酸钾、二氧化锰和氧气;
实验室制取气体时要按照一定的步骤进行;
(4)根据空气中各种物质的沸点不同,可以通过物理方法分离它们;
(5)过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,根据氧气的质量可以计算过氧化氢的质量.
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)高锰酸钾受热时容易扩散,分解能生成锰酸钾、二氧化锰和氧气;
实验室制取气体时要按照一定的步骤进行;
(4)根据空气中各种物质的沸点不同,可以通过物理方法分离它们;
(5)过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,根据氧气的质量可以计算过氧化氢的质量.
解答:解:(1)a是试管,常用作反应的容器;b是长颈漏斗,可以通过长颈漏斗向锥形瓶中注入液体.
故填:试管;长颈漏斗.
(2)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
反应不需要加热,应该用B装置作为发生装置.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;B.
(3)高锰酸钾受热分解的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;
因为氧气不易溶于水,可以用排水法收集,即用E装置收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
主要的实验步骤为:先检查装置气密性,再装药品并固定试管,再加热,再用排水法收集氧气,再将导管从水槽中取出,再停止加热,即顺序是③②①④⑥⑤.
故填:2KMnO4
K2MnO4+MnO2+O2↑;C;③②①④⑥⑤.
(4)氧气的沸点是-183℃,氮气的沸点是-196℃,因此根据氧气、氮气的沸点不同,工业上可以用分离液态空气的方法制取氧气.
故填:沸点.
(5)解:设分解的过氧化氢的质量为x,
2H2O2
2H2O+O2↑,
68 32
x 16g
=
,
x=34g,
故填:34.
故填:试管;长颈漏斗.
(2)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
反应不需要加热,应该用B装置作为发生装置.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;B.
(3)高锰酸钾受热分解的化学方程式为:2KMnO4
| ||
因为氧气不易溶于水,可以用排水法收集,即用E装置收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
主要的实验步骤为:先检查装置气密性,再装药品并固定试管,再加热,再用排水法收集氧气,再将导管从水槽中取出,再停止加热,即顺序是③②①④⑥⑤.
故填:2KMnO4
| ||
(4)氧气的沸点是-183℃,氮气的沸点是-196℃,因此根据氧气、氮气的沸点不同,工业上可以用分离液态空气的方法制取氧气.
故填:沸点.
(5)解:设分解的过氧化氢的质量为x,
2H2O2
| ||
68 32
x 16g
| 68 |
| 32 |
| x |
| 16g |
x=34g,
故填:34.
点评:本题主要考查制取气体时装置的选择、化学方程式的书写及其根据化学方程式进行计算,书写化学方程式时要注意规范性,特别是要注意配平,计算时要注意规范性和准确性.

练习册系列答案
相关题目