题目内容
【题目】根据下表回答问题:
温度/℃ | 20 | 40 | 60 | |
溶解度 | NaCl | 36.0 | 36.6 | 37.3 |
| 31.6 | 63.9 | 110 | |
(1)60℃,100g水中最多能溶解![]() 的质量为__________。
的质量为__________。
(2)下列说法正确的是_________(填序号)。
A.20℃时,![]() 饱和溶液的质量分数为31.6%
饱和溶液的质量分数为31.6%
B.40℃时,136.6gNaCl溶液中一定含有36.6gNaCl
C.将40℃时![]() 的饱和溶液降温到20℃,析出32.3g
的饱和溶液降温到20℃,析出32.3g![]() 固体
固体
D.将40℃时NaCl和![]() 的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>
的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>![]()
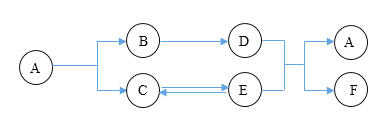
(3)20℃时,按下列图示操作:
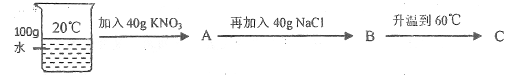
①在溶液A、B、C中,![]() 溶解达到饱和状态的有_______(填字母)。
溶解达到饱和状态的有_______(填字母)。
②比较溶液A、B中![]() 的质量分数:A_______B(填“>“或” <”或“=”)。
的质量分数:A_______B(填“>“或” <”或“=”)。
【答案】 110g D AB >
【解析】(1)固体物质的溶解度是指在一定温度下,100g溶剂里最多能溶解的某固体物质的质量,60℃时,100g水中最多能溶解110g硝酸钾。(2)A.20℃时,![]() 的溶解度是31.6g,则KNO3饱和溶液的溶质质量分数为:
的溶解度是31.6g,则KNO3饱和溶液的溶质质量分数为:![]() ×100%≠31.6%,错误;B.40℃时,136.6gNaCl饱和溶液中一定含有36.6gNaCl,若为指明溶液的状态,则无法求算溶质的质量,错误;C.将40℃时100g溶剂所形成的
×100%≠31.6%,错误;B.40℃时,136.6gNaCl饱和溶液中一定含有36.6gNaCl,若为指明溶液的状态,则无法求算溶质的质量,错误;C.将40℃时100g溶剂所形成的![]() 饱和溶液降温到20℃,折出32.3g
饱和溶液降温到20℃,折出32.3g![]() 固体,未指明饱和溶液的质量,无法求算析出晶体的质量,错误;D.将40℃时NaCl和
固体,未指明饱和溶液的质量,无法求算析出晶体的质量,错误;D.将40℃时NaCl和![]() 的饱和溶液分别降温至20℃,溶解度都变小,由于20℃时,NaCl的溶解度大于KNO3的溶解度,所以降温后两溶液质量分数的大小关系为NaCl>
的饱和溶液分别降温至20℃,溶解度都变小,由于20℃时,NaCl的溶解度大于KNO3的溶解度,所以降温后两溶液质量分数的大小关系为NaCl>![]() ,正确。故选D。(3)①20℃时,KNO3的溶解度是31.6g,一种溶剂中可同时溶解多种溶质,且互相不影响,所以A、B是KNO3的饱和溶液。60℃时,KNO3的溶解度是110g,C是KNO3的不饱和溶液,故填AB。②一种溶剂中可同时溶解多种溶质,且互相不影响,溶液B中由于多溶解了40gNaCl,所以溶液B比溶液A的质量多40g,但两溶液中溶解KNO3的质量相等,因此溶液A、B中
,正确。故选D。(3)①20℃时,KNO3的溶解度是31.6g,一种溶剂中可同时溶解多种溶质,且互相不影响,所以A、B是KNO3的饱和溶液。60℃时,KNO3的溶解度是110g,C是KNO3的不饱和溶液,故填AB。②一种溶剂中可同时溶解多种溶质,且互相不影响,溶液B中由于多溶解了40gNaCl,所以溶液B比溶液A的质量多40g,但两溶液中溶解KNO3的质量相等,因此溶液A、B中![]() 的质量分数是:A>B。
的质量分数是:A>B。

 阅读快车系列答案
阅读快车系列答案【题目】小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
(探究目的)探究所得溶液的酸碱性。
(提出猜想)所得溶液可能呈碱性,也可能呈______性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变 ______ | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈 ______ |
(分析与思考)
(1)若溶液呈碱性,为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入______溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为______。
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入金属锌,若观察到______,则所取溶液星酸性;若无明显现象,则呈中性。
方案二:取样,加入碳酸钠溶液,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为______,若无明显现象,则呈中性。
(3)工业上常用氢氧化钠来中和废水中的盐酸,现取废液50g,逐滴滴入10%的氢氧化钠溶液中和,当溶液pH为7时,用去氢氧化钠溶液8g。请计算废水中氯化氢的质量分数______。