题目内容
【题目】如图为A、B、C三种物质的溶解度曲线,据图回答:
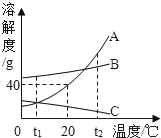
(1)t1℃时,三种物质的溶解度由大到小的关系为_____;
(2)20℃时,将25gA物质放入50g水中,充分搅拌,所得溶液的质量是_____g。
(3)若将t1℃三种物质的饱和溶液分别升温到t2℃时,则三种溶液中溶质的质量分数由小到大的顺序是_____。
(4)若将t2℃时C的饱和溶液降温到20℃时,发生改变的是_____。
a、溶剂质量b、溶质质量c、溶质质量分数d、溶解度
(5)20℃时,将接近饱和的B溶液变为饱和溶液,可采用_____方法(填一种方法就可)。
【答案】B>A=C 70 C<A<B d 加B物质的方法(或恒温蒸发溶剂)
【解析】
(1)根据A、B、C三种物质的溶解度曲线,t1℃时,三种物质的溶解度由大到小的关系为B>A=C;
(2)20℃时,A物质溶解度为40g,此时50g水中最多能溶解20gA物质,将25gA物质放入50g水中,充分搅拌,所得溶液的质量是20g+50g=70g。
(3)将t1℃三种物质的饱和溶液分别升温到t2℃时, A和B的溶质质量分数不变,C析出晶体,溶质质量分数减小,又t1℃时,三种物质的溶解度由大到小的关系为B>A=C,根据饱和溶液溶质质量分数= ![]() ,相同温度下,溶解度越大,饱和溶液溶质质量分数越大,故将t1℃三种物质的饱和溶液分别升温到t2℃时,其三种溶液中溶质的质量分数由小到大的顺序是C<A<B;
,相同温度下,溶解度越大,饱和溶液溶质质量分数越大,故将t1℃三种物质的饱和溶液分别升温到t2℃时,其三种溶液中溶质的质量分数由小到大的顺序是C<A<B;
(4)C的溶解度随温度降低而增大,若将t2℃时C的饱和溶液降温到20℃时,C的溶解度增大,溶剂质量、溶质质量、溶质质量分数均不变;
故填:d;
(5)20℃时,将接近饱和的B溶液变为饱和溶液,可增加溶质、减少溶剂,可采用加B物质的方法(或恒温蒸发溶剂)。

 习题精选系列答案
习题精选系列答案【题目】某化学兴趣小组为鉴别稀盐酸、稀硫酸、Ba(OH)2溶液、Na2CO3溶液和NaCl溶液五瓶无标签的溶液时,将它们随意编号为A、B、C、D、E后进行如下实验:

(1)根据以上实验过程,确定A溶液是_____,C溶液是_____,B、E混合时的现象为:_____;
(2)鉴别后把所有物质混合倒入同一烧杯中,最后发现混合物呈浑浊状,过滤后,滤液呈红色。说明滤液呈_____性,则滤渣的成分是_____;
(3)为了防止滤液污染环境,兴趣小组的同学对滤液的成分展开了探究。
(提出问题)红色滤液中含有的溶质除了石蕊和_____一定存在外,还有什么?
(提出猜想)猜想1:HCl;猜想2:H2SO4;猜想3:H2SO4和_____;猜想4:HCl和_____;猜想5:HCl和Na2SO4等猜想。
(设计方案)
实验方案 | 现象 | 结论 |
取少量红色滤液于试管中加入_____(只加一种物质) | 先有气泡生成,后有白色沉淀,溶液由红色变为蓝色 | 猜想4正确 |