题目内容
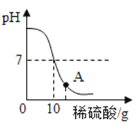
【题目】某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
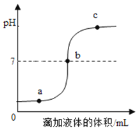
A. 该实验是将氢氧化钠溶液滴入稀盐酸中
B. a点所示溶液中,溶质只有NaCl
C. b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D. 向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
【答案】B
【解析】
根据溶液pH值的变化趋势,可知该实验是往稀盐酸中逐渐滴加氢氧化钠溶液,pH为7时,表示盐酸和氢氧化钠恰好完全反应。
A、根据溶液pH值的变化趋势,可知该实验是往稀盐酸中逐渐滴加氢氧化钠溶液,不符合题意;B、a点所示溶液中,溶质有盐酸和氢氧化钠反应生成的氯化钠,还有没反应的盐酸,错误,符合题意;C、b点表示稀盐酸和氢氧化钠溶液恰好完全反应,b点表示稀盐酸和氢氧化钠溶液恰好完全反应;D、c点溶液的pH大于7,溶液显碱性,滴加紫色石蕊试液,溶液变蓝,不符合题意。故选B。

 计算高手系列答案
计算高手系列答案【题目】某兴趣小组同学进行溶液的导电性实验研究。
(查阅资料)
(1)溶液的导电性是指溶液传导电流的能力。溶液导电是因为溶液中存在大量自由移动的离子
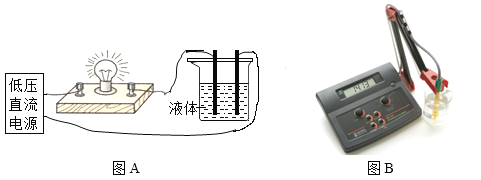
(2)利用图A所示的装置试验溶液的导电性,灯泡越亮,表示溶液的导电性越强。
(3)溶液的导电性也可以用电导率仪(如图B)测定出的电导率数值大小进行衡量。电导率数值越大,溶液的导电性越强。
(提出问题1)溶液是否都能导电?
(进行实验1)25℃时,用图A装置进行如下三个实验。
实验编号 | 液体 | 现象 | 实验结论与解释 | |
1-1 | 100mL水 | 灯泡不亮 | 水不导电 | |
1-2 | 100mL 10%的硝酸钾溶液 | 灯泡亮 | 硝酸钾溶液能导电 | 溶解在水中的硝酸钾能够解离出自由移动的k+和NO3- |
1-3 | 100mL 10%的蔗糖溶液 | 灯泡不亮 | 蔗糖溶液不导电 | 溶解在水中的蔗糖不能解离出自由移动,仍以蔗糖分子形式存在 |
(提出问题2)溶液的导电性是否受溶液浓度和温度的影响?
(进行实验2-1)30℃时,测定不同浓度氯化钠溶液的电导率,将数据记录下表。
氯化钠溶液浓度(%) | 1.4 | 2.8 | 4.2 | 5.6 | 7.0 |
电导率值(S/m) | 2.000 | 3.219 | 4.533 | 5.800 | 7.133 |
(进行实验2-2)
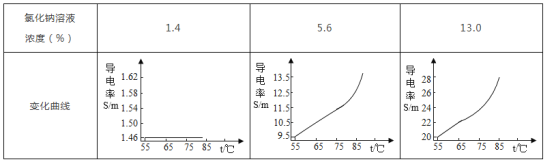
(解释与结论)
(1)实验1-1的目的是________。
(2)通过实验1-2和实验1-3的对比,说明________对溶液的导电性有影响。
(3)实验2-1中,溶解在水中的氯化钠解离出的离子是_______和______,分析实验数据,能够得出的结论是________。
(4)根据实验2-2,不能够得出“对于氯化钠溶液来说,温度越高,溶液的导电性越强”原因是_______。
(反思与交流)
(5)完成实验1-3后,有同学认为没有必要做实验1-1,理由是_________。