题目内容
【题目】根据题中给出的信息填空
(1)空气中体积分数约为21%的气体是____。
(2)地壳中含量最多的金属元素所形成的氧化物的化学式___。
(3)配制农药波尔多液所用硫酸铜的阴离子粒子是___(填化学符号)。
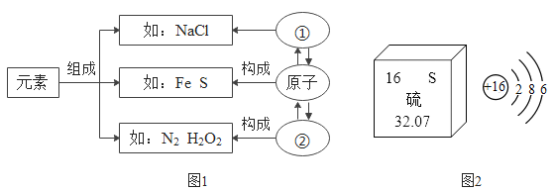
(4)元素周期表是学习和研究化学的重要工具.A、B、C为周期表1﹣18号中的元素,在周期表中的位置如图所示.已知A元素的单质是空气的主要成分之一,三种元素的核电荷数之和为31。
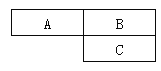
①A元素的名称为:_____.
②B元素单质的一种用途为_____.
【答案】氧气 Al2O3 SO42- 氮 供给呼吸
【解析】
(1)空气中体积分数约为21%的气体是氧气。
(2)地壳中含量最多的金属元素是铝元素,铝元素所形成的氧化物是氧化铝,化学式为Al2O3。
(3)配制农药波尔多液所用硫酸铜的阴离子粒子是硫酸根离子,硫酸根离子表示为SO42-。
(4)A、B、C为周期表1﹣18号中的元素,根据三种元素在周期表中的位置,已知A元素的单质是空气的主要成分之一,可能为氮元素或氧元素;对于原子来说,原子序数=核电荷数=核内质子数,故三种元素的核电荷数之和为31,即为三种元素的原子序数之和等于31;若A为氧元素,其原子序数为8,A、B同周期且相邻,B为氟元素,则B的原子序数为9,BC同主族,原子序数C比B多8,则C为氯元素,原子序数为17,三种元素的原子序数之和=8+9+17=34,不符合题意;假设A为氮元素,原子序数为7,B为氧元素,原子序数为8,BC同主族,原子序数C比B多8个,则C为硫元素,原子序数为16,三种元素的原子序数之和=7+8+16=31,符合题意。①A元素的名称为氮;②B元素为氧元素,其单质为氧气,用途为供给呼吸等。

【题目】某化学小组为测定大理石中碳酸钙的含量,称取大理石样品25.0g,分成五等份于5个烧杯中进行实验,记录有关实验数据如下表所示(大理石中其它成分均不溶于水,也不参加反应),计算:
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入大理石样品的质量/g | 5.0 | 5.0 | 5.0 | 5.0 | 5.0 |
加入稀盐酸的质量/g | 10.0 | 20.0 | 30.0 | 40.0 | 50.0 |
烧杯中剩余固体的质量/g | 4.0 | 3.0 | 2.0 | 1.0 | 1.0 |
(1)样品中碳酸钙的质量是 。
(2)所用稀盐酸的溶质质量分数。