题目内容
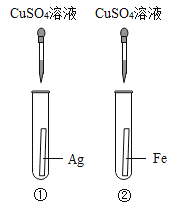
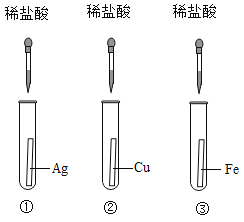
【题目】为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。
(1)能验证三种金属活动性顺序的方案是____________(填“A”或“B”)。
(2)方案A中,发生反应的化学方程式是________________。
(3)方案B中,证明铁的活动性比铜强的现象是_______________。
方案A | 方案B |
|
|
【答案】A Fe+CuSO4=FeSO4+Cu 铁能与稀盐酸反应生成气体,铜与稀盐酸不能反应
【解析】
(1)银与CuSO4溶液不反应,说明了活动性:铜>银;铁与CuSO4溶液反应置换出铜,说明了活动性:铁>铜;由此可得出三种金属活动性铁>铜>银。铁能与稀盐酸反应生成氢气,铜、银均不能与稀盐酸反应,无法确定银和铜的活动性强弱。能验证三种金属活动性顺序的方案是A;
(2)方案A中,铁与CuSO4溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为Fe+CuSO4=FeSO4+Cu;
(3)方案B中,证明铁的活动性比铜强的现象是铁能与稀盐酸反应生成气体,铜与稀盐酸不反应。

练习册系列答案
相关题目