题目内容
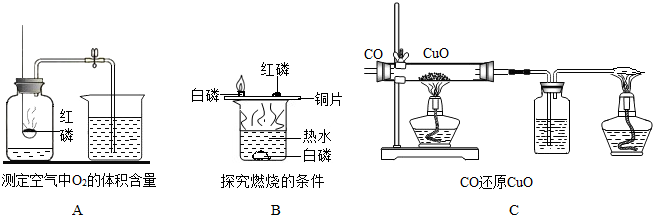
(2013?闵行区一模)下列是初中化学部分重要的实验或实验装置.请按要求填空:?
(1)A实验如果实验数据小于
,可能原因是
(2)B实验中水的作用是
(3)C中硬质玻璃管内发生反应的化学方程式为
(1)A实验如果实验数据小于
| 1 |
| 5 |
红磷的量太少(或装置的气密性不好、未冷却到室温就打开夹子)
红磷的量太少(或装置的气密性不好、未冷却到室温就打开夹子)
(写出一点),?该反应的化学方程式为4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
(2)B实验中水的作用是
提供热量,隔绝氧气
提供热量,隔绝氧气
;铜片上的现象是白磷燃烧,产生大量白烟,放热,红磷不燃烧
白磷燃烧,产生大量白烟,放热,红磷不燃烧
,由此得出可燃物燃烧的条件之一是温度要达到可燃物的着火点
温度要达到可燃物的着火点
.(3)C中硬质玻璃管内发生反应的化学方程式为
CO+CuO
Cu+CO2
| ||
CO+CuO
Cu+CO2
,右边酒精灯的作用是
| ||
燃烧掉多余的CO,防止污染空气
燃烧掉多余的CO,防止污染空气
.
分析:(1)根据测定空气中氧气的体积分数的实验原理、装置的特点、实验注意事项等分析误差;红磷和氧气反应生成了五氧化二磷,可以据此写出化学方程式;
(2)通过比较水中和空气中白磷的燃烧的情况,及空气中白磷和红磷燃烧情况,可以得出燃烧的条件及热水的作用;
(3)根据装置完成炼铜的原理的书写并根据一氧化碳的作用分析酒精灯的作用.
(2)通过比较水中和空气中白磷的燃烧的情况,及空气中白磷和红磷燃烧情况,可以得出燃烧的条件及热水的作用;
(3)根据装置完成炼铜的原理的书写并根据一氧化碳的作用分析酒精灯的作用.
解答:解:(1)测定空气中氧气含量的实验中,气体减少的体积小于l/5的可能原因:(1)红磷的量不足,瓶内氧气没有耗尽;(2)装置漏气(如塞子未塞紧、燃烧匙与橡皮塞之间有缝隙等),使外界空气进入瓶内;(3)未冷却至室温就打开弹簧夹,使进入瓶内的水的体积减少等;红磷和氧气反应生成了五氧化二磷,故化学方程式为:4P+5O2
2P2O5
(2)通过比较水中和空气中白磷的燃烧的情况,可以知道热水是用来隔绝空气,并对铜片上的白磷和红磷进行加热的;
铜片上的现象是:白磷燃烧,产生大量白烟,放热,红磷不燃烧;通过比较空气中白磷和红磷燃烧情况,可以得出燃烧的条件之一为达到物质燃烧的最低温度,即着火点;
(3)该反应原理为一氧化碳和氧化铜反应,该反应生成了二氧化碳和铜,反应的方程式为:CO+CuO
Cu+CO2;在该实验中利用了一氧化碳的可燃性用酒精灯来点燃尾气,防止一氧化碳对空气的污染.
故答案为:(1)红磷的量太少(装置的气密性不好、未冷却到室温就打开夹子);4P+5O2
2P2O5
(2)提供热量,隔绝氧气;白磷燃烧,产生大量白烟,放热,红磷不燃烧;温度要达到可燃物的着火点;
(3)CO+CuO
Cu+CO2;燃烧掉多余的CO,防止污染空气.
| ||
(2)通过比较水中和空气中白磷的燃烧的情况,可以知道热水是用来隔绝空气,并对铜片上的白磷和红磷进行加热的;
铜片上的现象是:白磷燃烧,产生大量白烟,放热,红磷不燃烧;通过比较空气中白磷和红磷燃烧情况,可以得出燃烧的条件之一为达到物质燃烧的最低温度,即着火点;
(3)该反应原理为一氧化碳和氧化铜反应,该反应生成了二氧化碳和铜,反应的方程式为:CO+CuO
| ||
故答案为:(1)红磷的量太少(装置的气密性不好、未冷却到室温就打开夹子);4P+5O2
| ||
(2)提供热量,隔绝氧气;白磷燃烧,产生大量白烟,放热,红磷不燃烧;温度要达到可燃物的着火点;
(3)CO+CuO
| ||
点评:本题考查了空气成分的测定、燃烧条件的探究及金属的冶炼等,想解答好这类题目,首先,要理解和熟记与之相关的知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能解答即可.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目


