题目内容
在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:(1)猜想与假设
甲认为有H2、CO生成;乙认为有H2、CO、CO2生成;
丙认为除有H2、CO、CO2外,可能还有N2生成.
探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是
(2)设计实验
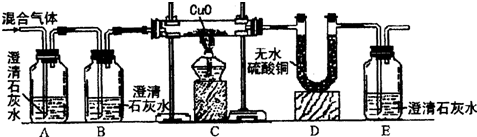
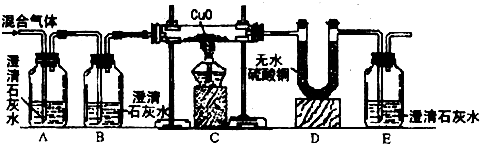
甲乙同学为了证明他们的猜想是正确的,设计了如图所示的实验装置:
(提示:无水硫酸铜遇到水变蓝色.)
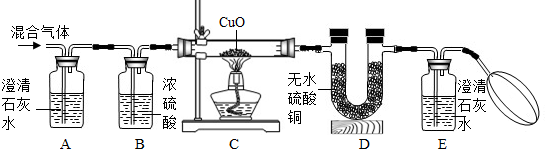
①A中澄清石灰水变浑浊,说明混合气体中含有
②证明混合气体中含有H2,相应的反应现象是
③证明混合气体中含有CO,相应的反应现象是
(3)反思与评价
①写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式
②丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装
分析:(1)根据质量守恒定律的微观解释分析解答,化学反应前后元素的种类不变,
(2)①检验二氧化碳常用澄清石灰水,
②根据氢气还原氧化铜生成的水会使无水硫酸铜变蓝的性质检验,
③根据一氧化碳还原氧化铜生成的二氧化碳会使澄清石灰水变浑浊的性质检验,
(3)①结合反应物、生成物和反应条件书写方程式,
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对一氧化碳的检验产生影响.
(2)①检验二氧化碳常用澄清石灰水,
②根据氢气还原氧化铜生成的水会使无水硫酸铜变蓝的性质检验,
③根据一氧化碳还原氧化铜生成的二氧化碳会使澄清石灰水变浑浊的性质检验,
(3)①结合反应物、生成物和反应条件书写方程式,
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对一氧化碳的检验产生影响.
解答:解:(1)在化学反应前后,元素的种类是不发生改变的,反应前的物质中没有氮元素,生成物中也不会有氮元素,所以水和碳反应后不会生成氮气,
故答案为:质量守恒定律,
(2)①二氧化碳能使澄清石灰水变浑浊,根据石灰水变浑浊的现象,可以确定混合其中存在二氧化碳,故答案为:CO2,
②水能够使无水硫酸铜变蓝,氢气和氧化铜反应会生成水,只要D中的无水硫酸铜变蓝,就证明水的存在,也证明了混合气中有氢气,
故答案为:D中硫酸铜变成蓝色物质,
③二氧化碳能使澄清石灰水变浑浊,一氧化碳和氧化铜反应会生成二氧化碳,只要澄清石灰水变浑浊,证明了二氧化碳的存在,也证明了混合气中有一氧化碳,
故答案为:E中澄清石灰水变浑浊,
(3)①根据焦炭和水在高温条件下生成氢气和一氧化碳,书写化学方程式,故答案为:C+H2O
CO+H2,
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对后面的一氧化碳的检验产生影响,氢氧化钠吸收二氧化碳比较完全,故答案为:NaOH.
故答案为:质量守恒定律,
(2)①二氧化碳能使澄清石灰水变浑浊,根据石灰水变浑浊的现象,可以确定混合其中存在二氧化碳,故答案为:CO2,
②水能够使无水硫酸铜变蓝,氢气和氧化铜反应会生成水,只要D中的无水硫酸铜变蓝,就证明水的存在,也证明了混合气中有氢气,
故答案为:D中硫酸铜变成蓝色物质,
③二氧化碳能使澄清石灰水变浑浊,一氧化碳和氧化铜反应会生成二氧化碳,只要澄清石灰水变浑浊,证明了二氧化碳的存在,也证明了混合气中有一氧化碳,
故答案为:E中澄清石灰水变浑浊,
(3)①根据焦炭和水在高温条件下生成氢气和一氧化碳,书写化学方程式,故答案为:C+H2O
| ||
②氢氧化钙的溶解度较小除去二氧化碳不彻底,会对后面的一氧化碳的检验产生影响,氢氧化钠吸收二氧化碳比较完全,故答案为:NaOH.
点评:本题主要考查了常见气体的检验和除杂方法,以及质量守恒定律在在化学方程式中的应用.

练习册系列答案
相关题目