题目内容
在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,探究小组同学作了如下探究:(1)猜想与假设
甲认为有H2、CO生成;
乙认为有H2、CO、CO2生成;
丙认为除有H2、CO、CO2外,可能还有N2生成.
探究小组组长丁认为丙同学的猜想不合理,丁同学做出判断的理论依据是
(2)设计与实验
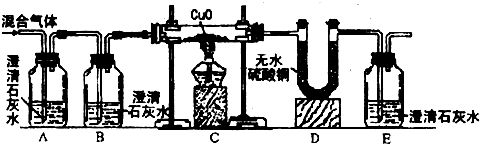
甲乙同学为了证明他们的猜想是正确的,设计了如如图所示的实验装置:
(提示:无水硫酸铜遇到水变蓝色,H2和CuO反应生成Cu和H2O,CO与CuO反应的原理与工业炼铁的反应原理相似.)
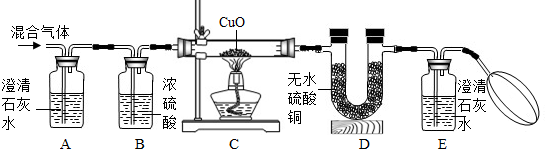
①证明混合气体中含有H2,相应的反应现象是
②证明混合气体中含有CO,相应的反应现象是
③证明混合气体中含有CO2,相应的反应现象是
(3)理论与思考
①写出符合甲同学猜想的焦炭与水蒸气发生反应的化学方程式
②丁同学认为此设计不够合理,如果在A、B装置之间再加一个洗气瓶,内装
分析:(1)根据质量守恒定律回答.
(2)根据H2、CO和氧化铜反应的产物和无水硫酸铜遇水变蓝色,以及二氧化碳能使澄清的石灰水变浑的性质回答.
(3)①根据甲的猜想,判断反应物、生成物和反应条件,再写出方程式;②根据氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好的情况回答.
(2)根据H2、CO和氧化铜反应的产物和无水硫酸铜遇水变蓝色,以及二氧化碳能使澄清的石灰水变浑的性质回答.
(3)①根据甲的猜想,判断反应物、生成物和反应条件,再写出方程式;②根据氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好的情况回答.
解答:解:(1)根据质量守恒定律,化学反应前后元素的种类不变,反应物中没有N元素,根据质量守恒定律不可能生成N2.
(2)①氢气和氧化铜在加热的条件下反应生成铜和水,一氧化碳与氧化铜反应生成铜和二氧化碳,如混合气体中含有H2,则
D中无水硫酸铜变蓝.
②一氧化碳与氧化铜反应生成铜和二氧化碳,如证明混合气体中含有一氧化碳,A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊.
③二氧化碳能使澄清的石灰水变浑,如混合气体中含有CO2,则A中澄清石灰水变浑浊.
(3)①甲认为在高温下炽热的焦炭能与水蒸气发生反应,其反应后的生成物有H2、CO,所以方程式为:C+H2O
H2+CO.
②氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好,在A、B装置之间再加一个洗气瓶,内装吸收二氧化碳能力较强的氢氧化钠溶液更好.
故答案为:(1)反应物中没有N元素,根据质量守恒定律不可能生成N2;
(2)①无水硫酸铜变蓝色;②A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊;③A中澄清石灰水变浑浊;
(3)①C+H2O
H2+CO;②NaOH.
(2)①氢气和氧化铜在加热的条件下反应生成铜和水,一氧化碳与氧化铜反应生成铜和二氧化碳,如混合气体中含有H2,则
D中无水硫酸铜变蓝.
②一氧化碳与氧化铜反应生成铜和二氧化碳,如证明混合气体中含有一氧化碳,A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊.
③二氧化碳能使澄清的石灰水变浑,如混合气体中含有CO2,则A中澄清石灰水变浑浊.
(3)①甲认为在高温下炽热的焦炭能与水蒸气发生反应,其反应后的生成物有H2、CO,所以方程式为:C+H2O
| ||
②氢氧化钙微溶解于水,溶液较稀,吸收二氧化碳的效果不好,在A、B装置之间再加一个洗气瓶,内装吸收二氧化碳能力较强的氢氧化钠溶液更好.
故答案为:(1)反应物中没有N元素,根据质量守恒定律不可能生成N2;
(2)①无水硫酸铜变蓝色;②A中澄清石灰水不变浑浊,E中澄清石灰水变浑浊;③A中澄清石灰水变浑浊;
(3)①C+H2O
| ||
点评:气体的检验和除杂是初中化学实验的重点内容之一,是学生应掌握的基本技能,也是化学实验考查的热点之一,首先要熟悉气体的性质,并能利用其性质对它进行检验、鉴别,能利用气体间性质的差别进行分离和除杂;特别是石灰水、氢氧化钠溶液、浓硫酸、无水硫酸铜在气体制取和检验中的作用.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案
相关题目