题目内容
化学的学习中会涉及到一些图形,根据不同图示所给信息回答下列问题:
(1)以如图所示实验都是我们曾经学习过的,请回忆实验过程回答下列问题: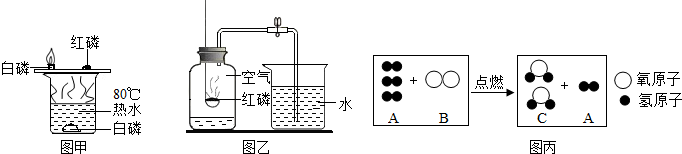
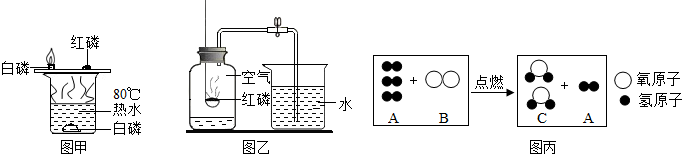
①图甲中能够得出“燃烧需要氧气”的现象是______,能够得出“燃烧需要使温度达到可燃物的着火点”的现象是______;当我们不需要燃烧时,根据燃烧的条件可以采用合理方法进行灭火.酒精灯不慎被打翻在实验桌上燃烧起来,常采用的灭火方法是______.
②某同学用图乙所示装置测定空气中氧气的含量,待红磷燃烧停止并冷却后,打开止水夹,观察到集气瓶中吸入水的体积约占集气瓶容积的______,若用木炭代替红磷来做这个实验,则向集气瓶中加入少量的______溶液,也可以达到实验目的.
(2)从微观的角度认识化学反应是学习化学的一种重要思维方式,如图丙是某反应听微观示意图,请分析图后回答:
①写出图丙所示的化学反应方程式______;
②该反应中参加反应的A、B的分子个数比为______.
解:(1)①燃烧需要氧气要通过对照实验,与氧气接触的物质燃烧了,与氧气不燃烧的不能燃烧,所以其它条件必须符合燃烧的条件,变量是与氧气是否接触,所以铜片上的白磷燃烧,热水中的白磷不燃烧,说明燃烧需要氧气;燃烧需要使温度达到可燃物的着火点,变量是温度是否达到着火点,其它条件必须符合燃烧的条件,所以铜片上的白磷燃烧,红磷不燃烧,说明红磷没有达到着火点;酒精灯不慎被打翻在实验桌上燃烧起来,可以用湿抹布盖灭,既隔绝了空气,又降低了温度;
②氧气约占空气体积的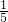 ,红磷燃烧消耗了氧气,在外界大气压的作用下,水进入集气瓶内,所以进入的水约占集气瓶体积的
,红磷燃烧消耗了氧气,在外界大气压的作用下,水进入集气瓶内,所以进入的水约占集气瓶体积的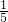 ;由于碳燃烧虽然消耗了氧气,但生成了二氧化碳属于气体,使瓶内气体压强保持不变,所以在瓶内放入氢氧化钠溶液,二氧化碳会被氢氧化钠溶液吸收,使瓶内气体压强减小,所以也能达到测定氧气体积的目的;
;由于碳燃烧虽然消耗了氧气,但生成了二氧化碳属于气体,使瓶内气体压强保持不变,所以在瓶内放入氢氧化钠溶液,二氧化碳会被氢氧化钠溶液吸收,使瓶内气体压强减小,所以也能达到测定氧气体积的目的;
(2)①反应物是氢气和氧气,生成物是水,用观察法配平,反应条件是点燃,所以方程式是:2H2+O2 2H2O;
2H2O;
②由于反应后还存在一个氢分子,所以说明三个氢分子中,只有两个氢分子参加了反应,消耗的氧分子是1个,所以参加反应的A、B的分子个数比为2:1.
故答案为:(1)①铜片上的白磷燃烧,热水中的白磷不燃烧;铜片上的白磷燃烧,红磷不燃烧;用湿抹布盖灭;②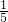 ;氢氧化钠;(2)①2H2+O2
;氢氧化钠;(2)①2H2+O2 2H2O;②2:1.
2H2O;②2:1.
分析:(1)①根据燃烧的条件和灭火的方法考虑;②根据氧气在空气中的体积含量考虑,二氧化碳能与氢氧化钠反应分析;(2)①根据微粒的构成和微粒个数写出方程式;②根据反应前后相同的分子是没有参加反应的分子考虑.
点评:解答本题关键是要熟悉燃烧的条件和灭火的方法,空气中氧气的含量,方程式的书写.
②氧气约占空气体积的
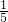 ,红磷燃烧消耗了氧气,在外界大气压的作用下,水进入集气瓶内,所以进入的水约占集气瓶体积的
,红磷燃烧消耗了氧气,在外界大气压的作用下,水进入集气瓶内,所以进入的水约占集气瓶体积的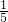 ;由于碳燃烧虽然消耗了氧气,但生成了二氧化碳属于气体,使瓶内气体压强保持不变,所以在瓶内放入氢氧化钠溶液,二氧化碳会被氢氧化钠溶液吸收,使瓶内气体压强减小,所以也能达到测定氧气体积的目的;
;由于碳燃烧虽然消耗了氧气,但生成了二氧化碳属于气体,使瓶内气体压强保持不变,所以在瓶内放入氢氧化钠溶液,二氧化碳会被氢氧化钠溶液吸收,使瓶内气体压强减小,所以也能达到测定氧气体积的目的;(2)①反应物是氢气和氧气,生成物是水,用观察法配平,反应条件是点燃,所以方程式是:2H2+O2
 2H2O;
2H2O;②由于反应后还存在一个氢分子,所以说明三个氢分子中,只有两个氢分子参加了反应,消耗的氧分子是1个,所以参加反应的A、B的分子个数比为2:1.
故答案为:(1)①铜片上的白磷燃烧,热水中的白磷不燃烧;铜片上的白磷燃烧,红磷不燃烧;用湿抹布盖灭;②
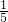 ;氢氧化钠;(2)①2H2+O2
;氢氧化钠;(2)①2H2+O2 2H2O;②2:1.
2H2O;②2:1.分析:(1)①根据燃烧的条件和灭火的方法考虑;②根据氧气在空气中的体积含量考虑,二氧化碳能与氢氧化钠反应分析;(2)①根据微粒的构成和微粒个数写出方程式;②根据反应前后相同的分子是没有参加反应的分子考虑.
点评:解答本题关键是要熟悉燃烧的条件和灭火的方法,空气中氧气的含量,方程式的书写.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目