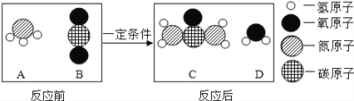
题目内容
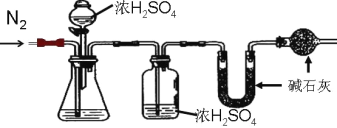
【题目】如图为实验室制取气体的常见装置。请回答:
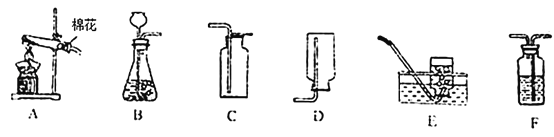
(1)写出用A装置制取氧气的化学方程式_____。
(2)若收集﹣瓶氧气用于完成铁丝在氧气中燃烧的实验最好用_____(填序号)装置收集氧气。
(3)实验室制取二氧化碳发生装置选择B的依据是_____,写出该反应的化学方程式_____。
(4)若用F装置干燥二氧化碳,瓶中应盛装_____。
【答案】 2KMnO4![]() K2MnO4+MnO2+O2↑ E 反应物是固体与液体,反应条件是常温; CaCO3+2HCl═CaCl2+H2O+CO2↑ 浓硫酸
K2MnO4+MnO2+O2↑ E 反应物是固体与液体,反应条件是常温; CaCO3+2HCl═CaCl2+H2O+CO2↑ 浓硫酸
【解析】
本题主要考查常见气体的发生装置的探究,发生装置依据反应物的状态和反应条件。
(1)装置A适用于固体加热制取氧气,试管口有一棉花团,所以是用热高锰酸钾制取氧气,高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4 ![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)在做铁丝在氧气中燃烧实验时,为了防止高温生成物溅落炸裂瓶底,需事先在瓶底放少量的水或铺一层细沙,用排水法收集时不将水完全排尽就可以,故选E;
(3)实验室制取二氧化碳用大理石和稀盐酸反应,选用发生装置B,大理石是固体,稀盐酸是液体,常温下反应,大理石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)浓硫酸具有吸水性且不能与二氧化碳反应,可用盛有浓硫酸的装置F来干燥二氧化碳。

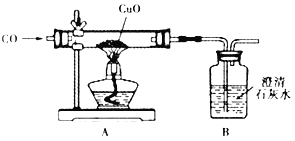
【题目】某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
(1)从安全环保的角度考虑,上述实验需要改进的是_____。
(2)装置A中发生反应的化学方程式为_____。
(3)同学们通过查阅资料得知:氧化亚铜(Cu2O)和铜均为红色固体,且Cu2O能和稀硫酸反应,反应的化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O.他们对反应后玻璃管中的红色固体进行如下探究:
(提出问题)反应后生成的红色固体成分是什么?
(作出猜想)猜想一:红色固体只有Cu
猜想二:红色固体只有Cu2O
猜想三:红色固体可能含有_____。
(实验探究)设计如下实验方案
实验操作 | 现象 | 结论 |
取少量红色固体于试管中,加入过量的稀硫酸。 | _____ | 红色固体含有Cu2O |
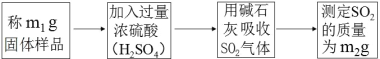
(思考与分析)甲同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是_____。为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,然后过滤、洗涤、干燥、称量,得到ng固体。当n>_____(含m的代数式)时,可以得出猜想三的结论正确。
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
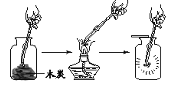
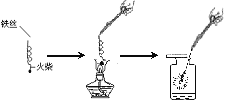
A 木炭燃烧 | B铁丝燃烧 |
(1)木炭在氧气中燃烧时,可观察到的实验现象为______________________。 (2)若验证生成物,需向集气瓶中加入的药品为_________________。 |
(1)铁丝在氧气中燃烧的化学方程式为_______。 (2)实验时,预先在集气瓶里装少量水的作用是_________________________。 |