题目内容
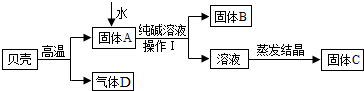
(2013?徐州一模)某校学生要进行一系列的实验,请结合下图帮助他们解决以下问题:
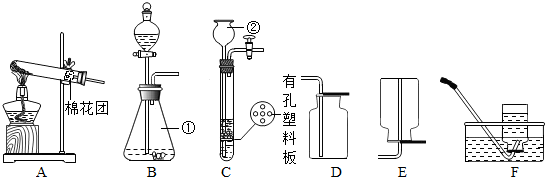
(1)图中标有②的仪器名称为
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是
(3)实验室制取氢气,选用的收集装置为
(4)用B、D装置可制取某种能使石灰水变浑浊的气体,制取该气体的化学方程式为
(5)已知浓盐酸具有挥发性,易挥发出氯化氢气体.浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M直接通人澄清石灰水中,石灰水没有变浑浊.据此事实估计,该气体M中应含有
(6)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.
①该反应的化学方程式是
②根据上述信息总结出氨气的性质有

(1)图中标有②的仪器名称为
长颈漏斗
长颈漏斗
;(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是
A
A
(填字母序号);(3)实验室制取氢气,选用的收集装置为
E或F
E或F
填字母序号);(4)用B、D装置可制取某种能使石灰水变浑浊的气体,制取该气体的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;(5)已知浓盐酸具有挥发性,易挥发出氯化氢气体.浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M直接通人澄清石灰水中,石灰水没有变浑浊.据此事实估计,该气体M中应含有
HCl、CO2、H2O
HCl、CO2、H2O
等成分;(6)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.
①该反应的化学方程式是
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
| ||
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
,收集氨气时应选用E装置,把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量红色液体进入;
| ||
②根据上述信息总结出氨气的性质有
密度比空气小、易溶于水等
密度比空气小、易溶于水等
(至少答2条).分析:据图即可知道仪器的名称,使用高锰酸钾制取氧气应该使用固体加热型发生装置;气体的收集装置取决于气体的水溶性和密度;能使澄清石灰水变浑浊的气体是二氧化碳;浓盐酸具有挥发性;加热氯化铵和氢氧化钙的固体能得到氯化钙、水和氨气,氨气的水溶液呈碱性,能使酚酞试液变红.
解答:解:(1)据图可知仪器是长颈漏斗,故填:长颈漏斗;
(2)加热高锰酸钾制取氧气应该选用固体加热型发生装置,故填:A;
(3)氢气的密度比空气小且很难溶于水,可以使用向下排空气法或排水法收集,故填:E或F;
(4)能使澄清石灰水变浑浊的气体是二氧化碳,实验室使用大理石或石灰石与稀盐酸反应,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(5)浓盐酸具有挥发性,能挥发出溶质氯化氢,氯化氢溶于水会形成盐酸,与石灰水中的溶质氢氧化钙发生反应而看不到溶液变浑浊的现象,故填:HCl、CO2、H2O;
(6)①氯化铵与氢氧化钙反应生成氯化钙、水和氨气,故填:2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑;
②选用E装置收集氨气,说明氨气的密度比空气小,集气瓶倒扣在滴有酚酞试液的水槽中,集气瓶内有大量液体进入,说明集气瓶内气体压强明显减小,即氨气易溶于水,水溶液使酚酞试液变红,说明溶液呈碱性,故填:密度比空气小、易溶于水等.
(2)加热高锰酸钾制取氧气应该选用固体加热型发生装置,故填:A;
(3)氢气的密度比空气小且很难溶于水,可以使用向下排空气法或排水法收集,故填:E或F;
(4)能使澄清石灰水变浑浊的气体是二氧化碳,实验室使用大理石或石灰石与稀盐酸反应,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(5)浓盐酸具有挥发性,能挥发出溶质氯化氢,氯化氢溶于水会形成盐酸,与石灰水中的溶质氢氧化钙发生反应而看不到溶液变浑浊的现象,故填:HCl、CO2、H2O;
(6)①氯化铵与氢氧化钙反应生成氯化钙、水和氨气,故填:2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑;
②选用E装置收集氨气,说明氨气的密度比空气小,集气瓶倒扣在滴有酚酞试液的水槽中,集气瓶内有大量液体进入,说明集气瓶内气体压强明显减小,即氨气易溶于水,水溶液使酚酞试液变红,说明溶液呈碱性,故填:密度比空气小、易溶于水等.
点评:本题考查了常见气体制取发生和收集装置的选择,完成此题,可以依据物质的性质进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目