题目内容
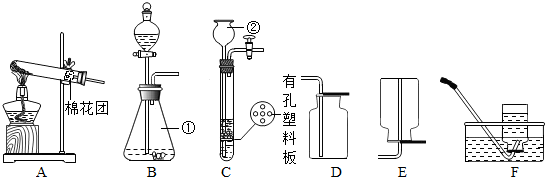
(2013?徐州一模)某小组同学按如图所示流程进行实验,用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,请你参与讨论并回答相关问题.
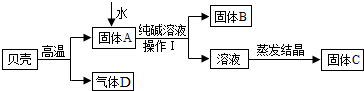
(1)贝壳高温煅烧时,发生反应的化学方程式是
(2)固体A和还原铁粉是食品包装袋中常用的两种干燥剂.
①可区分两种干燥剂的简单物理方法是
②气体D固态时的名称为
③操作I中用到的玻璃仪器有烧杯、
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是
【问题与发现】该小组同学所得到固体C一定是纯净的Na0H吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH;
乙:NaOH和Na2CO3的混合物;
丙:NaOH和Ca(OH)2:的混合物.
【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.他们的实验操作、现象和结论记录如下表,请参与他们的探究并完成所缺内容.
【反思与评价】根据实验流程,可以判定甲同学设计的方案不严密,理由是

(1)贝壳高温煅烧时,发生反应的化学方程式是
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
(2)固体A和还原铁粉是食品包装袋中常用的两种干燥剂.
①可区分两种干燥剂的简单物理方法是
用磁铁吸引
用磁铁吸引
;②气体D固态时的名称为
干冰
干冰
;③操作I中用到的玻璃仪器有烧杯、
漏斗
漏斗
、玻璃棒;(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是
使液体受热均匀,防止液滴外溅
使液体受热均匀,防止液滴外溅
;【问题与发现】该小组同学所得到固体C一定是纯净的Na0H吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH;
乙:NaOH和Na2CO3的混合物;
丙:NaOH和Ca(OH)2:的混合物.
【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.他们的实验操作、现象和结论记录如下表,请参与他们的探究并完成所缺内容.
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量 稀盐酸 稀盐酸 |
无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液 | 出现白色沉淀 出现白色沉淀 |
猜想成立 |
因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠
因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠
.分析:(1)煅烧碳酸钙时,碳酸钙分解能生成氧化钙和二氧化碳;
(2)磁铁能够吸引铁,不能吸引氧化钙;干冰是二氧化碳的固体;过滤时要用到的主要仪器之一是漏斗;
(3)玻璃棒的用途有搅拌、引流、转移物质等;
【探究与验证】
显碱性的溶液能使酚酞试液变红色,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
【反思与评价】
碳酸钠、氢氧化钙的水溶液都显碱性,都能够使酚酞试液变红色.
(2)磁铁能够吸引铁,不能吸引氧化钙;干冰是二氧化碳的固体;过滤时要用到的主要仪器之一是漏斗;
(3)玻璃棒的用途有搅拌、引流、转移物质等;
【探究与验证】
显碱性的溶液能使酚酞试液变红色,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
【反思与评价】
碳酸钠、氢氧化钙的水溶液都显碱性,都能够使酚酞试液变红色.
解答:解:(1)贝壳高温煅烧时,含有的碳酸钙受热分解生成氧化钙和二氧化碳,反应的化学方程式是:CaCO3
CaO+CO2↑.
故填:CaCO3
CaO+CO2↑.
(2)①可区分两种干燥剂的简单物理方法是:用磁铁吸引,能够被吸引的物质是铁,不能被吸引的物质是氧化钙.
故填:用磁铁吸引.
②气体D是二氧化碳,固态时的名称为干冰.
故填:干冰.
③操作I中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
故填:漏斗.
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是:使液体受热均匀,防止液滴外溅.
故填:使液体受热均匀,防止液滴外溅.
【探究与验证】
乙:取少量固体C,溶于适量水形成溶液后,滴加足量的稀盐酸,如果无气泡产生,说明氢氧化钠中不含有碳酸钠,猜想不成立.
故填:稀盐酸.
丙:取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液,如果出现白色沉淀,说明氢氧化钠中含有氢氧化钙,猜想成立.
故填:出现白色沉淀.
【反思与评价】根据实验流程,可以判定甲同学设计的方案不严密,理由是:因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠.
故填:因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠.
| ||
故填:CaCO3
| ||
(2)①可区分两种干燥剂的简单物理方法是:用磁铁吸引,能够被吸引的物质是铁,不能被吸引的物质是氧化钙.
故填:用磁铁吸引.
②气体D是二氧化碳,固态时的名称为干冰.
故填:干冰.
③操作I中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
故填:漏斗.
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是:使液体受热均匀,防止液滴外溅.
故填:使液体受热均匀,防止液滴外溅.
【探究与验证】
乙:取少量固体C,溶于适量水形成溶液后,滴加足量的稀盐酸,如果无气泡产生,说明氢氧化钠中不含有碳酸钠,猜想不成立.
故填:稀盐酸.
丙:取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液,如果出现白色沉淀,说明氢氧化钠中含有氢氧化钙,猜想成立.
故填:出现白色沉淀.
【反思与评价】根据实验流程,可以判定甲同学设计的方案不严密,理由是:因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠.
故填:因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.

练习册系列答案
相关题目