题目内容
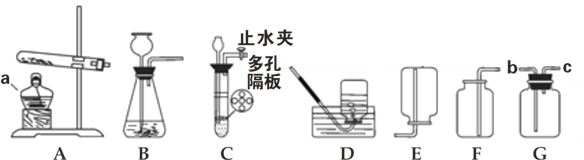
【题目】下列实验现象描述正确的是
A.二氧化碳气体通入紫色石蕊试液中,溶液变蓝色
B.电解水实验中与电源正、负极相连的电极上产生的气体体积之比为1∶2
C.铁丝在空气中燃烧,火星四射,生成黑色固体
D.点燃红磷后,产生大量的白雾
【答案】B
【解析】
试题分析:二氧化碳气体通入紫色石蕊试液中,溶液变红色,A错误;电解水实验中与电源正、负极相连的电极上产生的气体体积之比为1∶2,B正确;铁丝在空气中不能燃烧,C错误;点燃红磷后,产生大量的白烟,D错误。故选B。

【题目】下图是“XX牌贴身暖宝宝”使用说明书,小王等同学阅读了使用说明后,对它的成分和发热原理产生了兴趣,和同学们一起进行了实验探究。

(1)【初步探究成分及发热原理】
【提出问题】“暖宝宝”为什么能发热?
【做出猜想】“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程。
【设计实验】
实验操作 | 实验现象 | 解释或结论 | |
步骤1 | 取A、B两袋“暖宝宝”,将A袋按使用说明打开外袋取出内袋;而B袋不打开外袋。并将两袋样品放置在同样的环境中。 | A袋的“暖宝宝”温度很快上升;B袋温度_____。 | “暖宝宝”发热是由于袋内物质与__接触。 |
步骤2 | 24小时后,分别剪开A、B两袋,各取少量袋内物质于两支试管中,分别加入适量稀盐酸。 | A袋内物质部分溶解,产生黄色溶液;B袋内物质_____。 | 用化学方程式表示产生黄色溶液的反应 _____________________ |
【得出结论】 “暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程。 | |||
【继续探究】小王和同学们想继续探究“暖宝宝”发热后,剩余物质中是否还含有活性炭,他们取适量A袋内物质于烧杯内,加入过量_______,充分反应后过滤,洗涤、干燥滤渣。
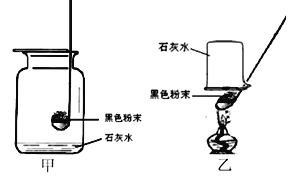
为进一步验证黑色滤渣的成分,小王和小李同学分别设计了甲、乙两个如图所示的装置,点燃滤渣,用澄清石灰水验证产物,你认为______图的装置结论更可靠,理由是______。
同学们分析铁生锈是一个缓慢氧化的过程,从原料角度分析“暖宝宝”放热现象之所以很明显是因为:
①铁呈粉末状,活性炭有吸附性,促使铁能与氧气、水等反应更快;②_____________;
(2)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验。
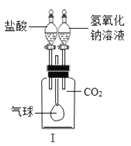
【实验方法】 取样品m g,利用如图丙所示装置与药品,测反应后生成气体的体积。
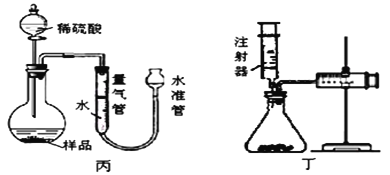
【实验步骤】① 连接仪器,_______;
② 将实验所用药品装入各仪器中,记录量气管初始刻度;
③ 打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出。在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管_____(填“上提”或“下移”);
④ 等恢复至室温,并_______________后,再次记录量气管刻度。
【数据处理】
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL。则该“暖宝宝”中铁粉的质量分数的表达式为________________。(用含dvm的字母表示)
【交流讨论】利用丙装置,即使操作无失误,测量结果仍会偏大,原因是__________,
小王重新设计了一个如图丁的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1 mL,充分反应后,右侧针筒中气体变化的读数为V2 mL,则反应生成的氢气的体积为_____________ mL。
(3)【测定“暖宝宝”中的氧化铁的含量】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,取10g袋内物质立即进行实验。
【查阅资料】① 2Fe(OH)3 ==![]() == Fe2O3 + 3H2O ② Fe + 2 FeCl3 = 3 FeCl2
== Fe2O3 + 3H2O ② Fe + 2 FeCl3 = 3 FeCl2
③ 在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】
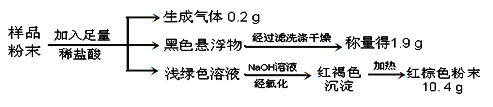
【实验结论】①写出产生气体的化学方程式_____________
②经该实验测定,该片已有破损的“暖宝宝”中的氧化铁的含量为 _____ 。(写出计算过程)
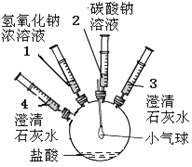
【题目】某实验小组的同学要探究酸碱盐中碳酸钠的化学性质,设计了如下实验装置及方案:
实验装置 | 实验步骤及操作 | 实验现象 |
| ①将注射器2中的溶液推入盛有稀盐酸的瓶中,至不再有气泡产生。 | 气球变瘪 |
②将注射器3稍稍向外拉 | 澄清石灰水变浑浊 | |
③将注射器1中的溶液推入瓶中 | 气球鼓起 | |
④将注射器4中的溶液推入瓶中 | 溶液变浑浊 |
(1)步骤①中气球变瘪的原因___________________________________________。
(2)步骤③中气球鼓起的原因____________________________________________。
(3)步骤④中发生反应的化学方程式______________________________________。