题目内容
【题目】某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示,
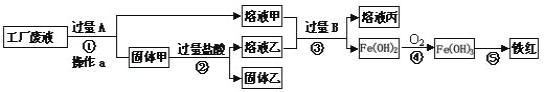
回答下列问题。
(1)固体甲_______,操作a的名称是_______。
(2)工厂废液中加入过量A反应的化学方程式为 。
(3)溶液甲中的金属离子是 (写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是 (填序号)。
【答案】(1)Fe、Cu 过滤
(2)Fe+CuCl2=FeCl2+Cu
(3)Na+、Fe2+
(4)①②
【物质组成和变化分析】
【解析】
试题分析:(1)求全过程不引入其他金属元素,则加入的过量A为金属为铁,铁将氯化铜中的铜置换出来,通过过滤后得到固体甲,固体甲中含有铁和铜;
(2)铁和氯化铜反应,生成氯化亚铁和铜;
(3)溶液甲中含有溶质氯化亚铁和氯化钠,则含有的金属离子是钠离子和亚铁离子;
(4)步骤①发生的反应是Fe+CuCl2=FeCl2+Cu,属于置换反应;步骤②发生的反应是Fe + 2 HCl==FeCl2 + H2↑,属于置换反应,步骤③发生的反应是:2NaOH+ FeCl2 ===== Fe(OH)2↓+ 2NaCl,属于复分解反应。故选①②

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目