题目内容
【题目】(2017唐山滦县一模)唐山市中考实验操作题鉴别NaOH、NaCl、HCl、Ca(OH)2四种溶液,给它们编号A、B、C、D。兴趣小组的同学小艾、小可分别取四种溶液,分别滴加Na2CO3溶液,鉴别出HCl和Ca(OH)2;然后用酚酞溶液鉴别出NaOH和NaCl。滴加Na2CO3溶液时发现所取B溶液有白色沉淀生成,过滤取该滤液探究其成分。
(作出猜想)他们认为滤液中一定有NaOH,理由____________(用化学方程式表示)。
对其他成分又分别作了如下猜想:
小艾猜想:还可能有________
小可猜想:还可能有Na2CO3
(进行实验)请你选择除CO2以外的物质,设计一个实验方案验证小艾的猜想(要求简述操作步骤、现象及结论):__________。
小可取一定量的溶液于试管中,向其中滴加了几滴稀盐酸,没有气泡,于是他便否认了自己的猜想。
(反思评价)小云认为小可的结论不严密,理由是______。
(拓展延伸)细心的小艾同学发现;鉴别完四种溶液后的6只试管中的废液倒入同一污物瓶,自己的污物瓶废液呈红色,小可的是无色澄清液体。于是继续探究无色澄清液体中溶质成分,除酚酞外一定还有________,可能有________,最后用_____________确定了可能有的物质确实存在,探究完后他们对酸碱盐知识有了更深刻的理解。
【答案】![]() Ca(OH)2 取少许滤液于试管中,滴加碳酸钠溶液,若出现白色沉淀,则证明滤液中含有氢氧化钙 加入的稀盐酸太少,若稀盐酸先与NaOH反应,不与碳酸钠反应,也不会出现气泡 NaCl HCl 紫色石蕊溶液(或铁粉、碳酸钠等,合理即可)
Ca(OH)2 取少许滤液于试管中,滴加碳酸钠溶液,若出现白色沉淀,则证明滤液中含有氢氧化钙 加入的稀盐酸太少,若稀盐酸先与NaOH反应,不与碳酸钠反应,也不会出现气泡 NaCl HCl 紫色石蕊溶液(或铁粉、碳酸钠等,合理即可)
【解析】
将碳酸钠溶液滴加到B溶液中有白色沉淀生成,因此可知B为氢氧化钙,其反应为碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,因此过滤后滤液中一定含有NaOH,可能含有碳酸钠或氢氧化钙,验证氢氧化钙存在时,可选择碳酸钠溶液,利用产生白色沉淀这一现象得出结论;在验证碳酸钠存在时,加入稀盐酸,根据酸碱优先反应的原理可知,滤液中一定含NaOH,因此滴加盐酸先与NaOH反应,再与碳酸钠反应产生气泡,因为滴加稀盐酸量太少时,可能少量的稀盐酸只与NaOH反应,不与Na2CO3反应,则无法确定碳酸钠的存在。【拓展延伸】实验后将六支试管中的废液混合后,由于小可得到的是无色澄清溶液,因此混合废液不可能显碱性,即氢氧化钠、碳酸钠和氢氧化钙都不可能存在,由于氯化钠未参加反应,因此一定含有氯化钠,可能含有HCl,检验盐酸存在的试剂很多,如紫色石蕊溶液、铁粉等活泼金属、碳酸钠等物质均可。

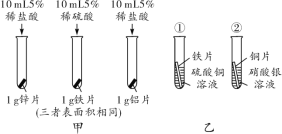
【题目】(2017石家庄桥西区模拟)化学小组的同学用如图甲所示装置进行木炭和氧化铜反应的实验,在进行实验时,他们首先将碳和氧化铜研磨成粉末,且混合均匀后,再开始实验,这样做的目的是___。充分反应后,化学小组的同学对试管内的固体成分进行了探究Ⅰ,对生成气体的成分进行了探究Ⅱ。按要求填空。
探究Ⅰ:试管内固体的成分是什么?
(作出猜想)猜想一:Cu;
猜想二:___;
猜想三:Cu和CuO。
(实验验证)
实验操作 | 实验现象 | 实验结论 |
取少量固体加入试管中,然后加入过量稀硫酸,振荡 | __ | 猜想三成立 |
固体和稀硫酸反应的化学方程式为______。
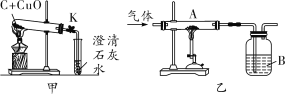
探究Ⅱ:生成的气体中是否含有一氧化碳?
通过如图甲的实验分析,生成的气体中一定含有二氧化碳,是否含有一氧化碳,小组同学进行了下列实验:
实验操作 | 实验现象 | 实验结论 |
收集碳和氧化铜反应生成的气体,除尽二氧化碳气体、干燥后,再将气体通入图乙装置中 | A中的红棕色粉末变成黑色,B中产生白色沉淀 | 生成气体中含有一氧化碳 |
则B中的溶液是__;A中反应的化学方程式为___。
(实验反思)图乙装置的缺陷是_____。