题目内容
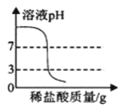
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述错误的是( )
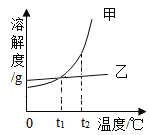
A.依据溶解度曲线可判断,t2℃时甲的溶解度比乙的大
B.将t2℃时甲的饱和溶液变为不饱和溶液,可采取升温的方法
C.将甲、乙的饱和溶液从t2℃降到t1℃,甲的析出质量比乙的多
D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
【答案】C
【解析】
A、依据溶解度曲线可判断,t2℃时甲的溶解度比乙的大,故A正确;
B、由溶度曲线可知,甲的溶解度随温度的升高而增大,溶解度增大,甲溶液可以变为不饱和溶液,故将t2℃时甲的饱和溶液变为不饱和溶液,可采取升温的方法,故B正确;
C、将甲、乙的饱和溶液从t2℃降到t1℃,析出质量的多少与溶液质量有关,甲乙溶液质量不确定无法比较析出溶质多少,故C错误;
D、t1℃时甲乙溶解度相等,饱和溶液溶质质量分数都等于![]() ,故溶质质量分数相等,溶液质量也相等为100g,所以溶质质量也相等等于
,故溶质质量分数相等,溶液质量也相等为100g,所以溶质质量也相等等于![]() ,D正确;
,D正确;
故选:C

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
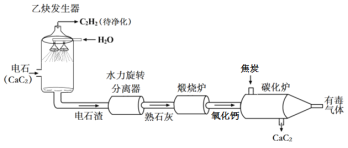
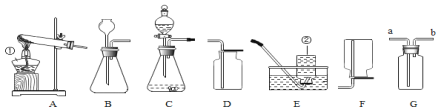
唐印文化课时测评系列答案【题目】同学们对烧烤用的“锡纸”产生了浓厚兴趣,那么“锡纸”中的金属是什么呢?
(猜想与假设)同学们结合金属的颜色、活动性、价格等因素。猜想:可能是锡、铝、镁、铁中的一种。
(查阅资料)
①氧化铝的熔点 2045℃;
②锡(Sn)与酸或盐溶液反应生成+2 价的锡盐;
③金属锌似晶体状,锌粉是一种深灰色固体,室温下,锌较硬且相当脆。
(初步探究)同学们结合金属的主要的物理和化学特性设计了如下实验:
序号 | 实验方案 | 现象 | 结论 |
1 | _____ | 无明显现象 | 金属不可能是铁 |
2 | 用坩埚钳夹取打磨后的“锡纸”条,放在酒精灯上点燃。 | “锡纸”条熔化但没有滴落,也没燃烧。 | 金属不可能是___ |
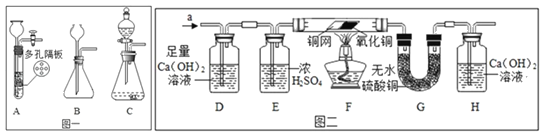
(深入探究)同学们对于“锡纸”到底是什么金属。进行了深入的实验探究。
第一组同学:(1)将“锡纸”条卷成和铁钉一样粗细,先在 20%的盐酸中浸泡至产生较多气泡,再取蒸馏水清洗,然后浸在蒸馏水中备用。
(2)将打磨后的铁钉和备用的“锡纸” 条分别放入到装有 5 mL 15%的稀盐酸中,观察到“锡纸”条表面产生的气泡速率比铁钉快。
(实验结论)制作“锡纸”的金属是_____。
第二组同学:取备用 的“锡纸”条放入试管中,滴加_____溶液,“锡纸”表面有深灰色固体析出,也得出和第一组相同的结论,写出它们的化学方程式_________________________。
(交流与反思)
(1)“锡纸”在酒精灯上加热,“锡纸”熔化但没有滴落的原因是_____。
(2)同学们在老师的帮助下,将 3 克烘干的备用“锡纸”片放入装有硫酸锌溶液的试管中,5 分钟后,取出“锡纸”片,洗涤、烘干、称量。反应后金属质量范围是_____。