题目内容
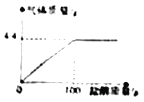
【题目】2020年南充市初中化学实验考题“酸性硫酸铜溶液与烧碱溶液反应”(酸性硫酸铜溶液就是硫酸与硫酸铜的混合溶液)同学们认真实验,操作规范、现象明显。此实验中某同学量取了10ml混合溶液,并逐滴向混合溶液中滴入烧碱溶液至反应刚好进行完全。实验中得到沉淀质量与滴入的烧碱溶液质量如图所示:
![]()
0
(1)若H2SO4和CuSO4混合溶液中Cu2+与SO![]() 的个数比为7:10。则溶液中H+与SO
的个数比为7:10。则溶液中H+与SO![]() 的个数比为多少。
的个数比为多少。
(2)如果混合溶液的密度为1.2g/ml,求混合溶液中硫酸铜的质量分数。(结果保留0.1%)。
【答案】(1)3:5(2)13.3%
【解析】
根据溶液中电荷守恒可得到H+与SO![]() 的个数比;再利用反应
的个数比;再利用反应![]() 中,氢氧化铜沉淀的质量,代入方程式进行作答。
中,氢氧化铜沉淀的质量,代入方程式进行作答。
(1)H2SO4和CuSO4混合溶液中有离子:H+、Cu2+、SO![]() 。溶液中电荷守恒有阳离子所带的正电荷总数和阴离子所带的负电荷总数相等,Cu2+与SO
。溶液中电荷守恒有阳离子所带的正电荷总数和阴离子所带的负电荷总数相等,Cu2+与SO![]() 的个数比为7:10,则设Cu2+的个数为7,SO
的个数比为7:10,则设Cu2+的个数为7,SO![]() 的个数为10,H+的个数为
的个数为10,H+的个数为![]() ,则有7×2+
,则有7×2+![]() =10×2,
=10×2,![]() =6,所以H+与SO
=6,所以H+与SO![]() 的个数比为6:10=3:5。
的个数比为6:10=3:5。
(2)解:设混合溶液中CuSO4的质量为![]() ,
,
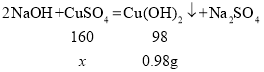
![]() ,解得:
,解得: ![]()
混合溶液中CuSO4的质量分数![]()
答:原混合溶液中硫酸铜的质量分数约为 13.3%。

 通城学典默写能手系列答案
通城学典默写能手系列答案【题目】由于“新冠”疫情,学校复课后,“二氧化氯”消毒液广泛应用于学校教室、食堂、寝室等的卫生消毒,某校决定今天放学后对全校教室、食堂、寝室等全面消毒。小陈观察到瓶上的标签如表所示。求:
二氧化氯1000mL | |
溶质的质量分数 | 80% |
密度 | 1.2g/cm3 |
强腐蚀性,阴冷,密封储藏 | |
(1)这1000毫升二氧化氯消毒液的质量是 ,其中含溶质二氧化氯 g。
(2)我校欲配制60kg质量分数为10%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少千克水?
【题目】溶液在工农业生产和人们的日常生活中有着重要的应用,请完成下列有关溶液的问题。
(1)把下列物质加入水中,充分搅拌能形成无色溶液的是__。(填编号)
①面粉 ②食盐 ③高锰酸钾 ④冰
(2)固体物质加入水中常常与水反应或溶解在水中。这些过程常伴随能量的转换。下列物质加入A试管中,U型管中a液面会升高的有___。(填编号)
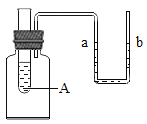
①浓H2SO4 ②NH4NO3③CaO
(3)疫情期间,人们常用75%的酒精消毒。75%的酒精是75体积的酒精(密度0.8g/ml)和25体积的水(密度1.0g/mL)混合而成。则该酒精溶液的溶质质量分数为___。(保留一位小数)
(4)喝下汽水会打嗝,说明气体在水中的溶解度和温度的关系是:___。
(5)NaCl和Na2CO3是生活中的两种重要物质。下面是两物质在不同温度时的溶解度及溶解度曲线。回答下列问题:
温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
NaCl溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
Na2CO3溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
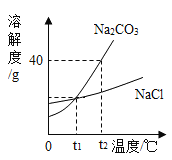
①从上图分析,NaC1和Na2CO3溶解度相等的温度是_________。
②将t2°C时等质量的NaCl和Na2CO3饱和溶液同时降温到t1°C。过滤得到NaCl晶体Ⅹ,Na2CO3晶体Y,NaCl滤液Q,Na2CO3滤液W。下列关于晶体和滤液的说法正确的是_____。
A X<Y
B 滤液中水:Q<W
C 滤液中溶质质量:Q=W