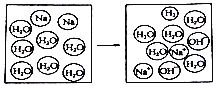
题目内容
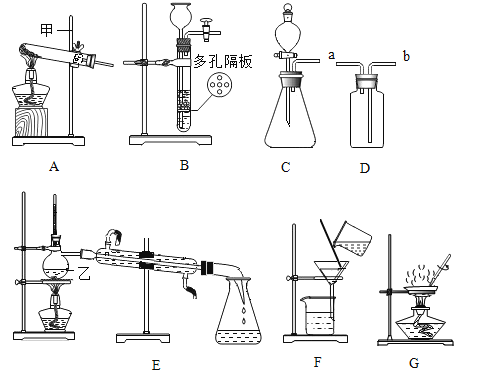
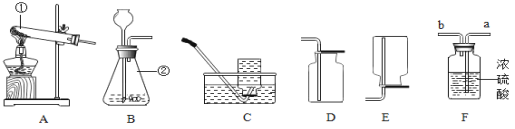
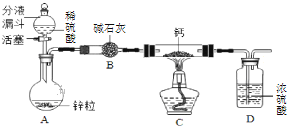
【题目】实验室利用如图所示实验装置进行有关化学实验,回答下列问题:
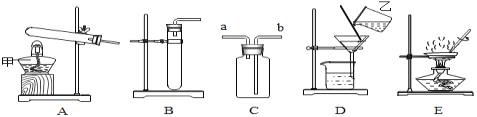
(1)写出图中仪器乙的名称:乙__________________。
(2)实验室用高锰酸钾制取氧气,发生装置可选择图中的_______________(填标号); 若实验室用B装置制取氧气,化学方程式是_________________,用充满水的装置C收集氧气,则氧气需从____________(填“a”或“b”)端通入
(3)实验室制取二氧化碳的化学方程式是____________,用装置C收集二氧化碳,验满时应将燃着的木条应放在________________(填“a”或“b”)端,检验二氧化碳的试剂是_________。
(4)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练。
①选择D装置对固液残留物进行过滤时玻璃棒的作用是_______________。
②取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的目的是_________。
【答案】烧杯 A 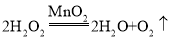 a CaCO3+2HCl=CaCl2+H2O+CO2↑ a 澄清的石灰水 引流 使液体受热均匀、防止液体因局部过热而飞溅
a CaCO3+2HCl=CaCl2+H2O+CO2↑ a 澄清的石灰水 引流 使液体受热均匀、防止液体因局部过热而飞溅
【解析】
(1)由装置图可知,b为烧杯;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,属于固体加热型所以选择装置A来制取;若选择B装置,不需要加热,则为双氧水在二氧化锰的催化下反应制氧气,化学方程式为: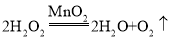 ;由于氧气不溶于水,用充满水的装置C收集氧气,则氧气需从短管进入,则从a端通入。
;由于氧气不溶于水,用充满水的装置C收集氧气,则氧气需从短管进入,则从a端通入。
(3)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;因为二氧化碳的密度比空气的密度大,因此长进短出,则用装置C收集二氧化碳,验满时,燃着木条应放在a端;二氧化碳一般用澄清的石灰水检验;
(4)对固液残留物进行过滤,因此选择D装置进行过滤时玻璃棒的作用是引流;取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的目的是使液体受热均匀、防止液体因局部过热而飞溅。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案【题目】某同学对CaH2的制备和性质进行探究。
(阅读资料)①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成Ca(OH)2和H2
③CaH2要密封保存,遇水反应也生成Ca(OH)2和H2
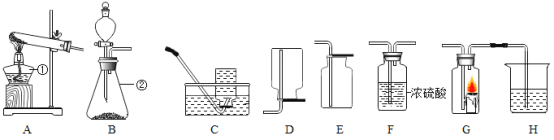
(CaH2的制备)设计的制取装置如图所示:
(1)装置B的作用是________________;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显__________色。该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是_______。
(CaH2的性质探究)
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。该同学进行了如下的探究。
(3)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因_________。
(实验验证)
实验 | 现象 | 结论 |
实验一:取滤液,向其中滴入少量 Na2CO3溶液 | ________ | 猜想二不成立 |
实验二:另取滤液,向其中加入足量稀盐酸 | ________ | 猜想三成立 |
(定量分析)
(4)取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2.4g,则该样品中CaH2的质量分数为____
(反思与交流)
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是氢化钙是固体,携带方便。既然金属钙与水反应也能生成氢气,为什么还要将金属钙制备成氢化钙呢?你的观点是:____。
(6)测量小组利用电子天平,采用如下图所示方法以反应前后失去的质量来求算CaH2纯度,结果纯度的测定值偏____。(填“偏低”“偏高”或“不变”)