题目内容
【题目】已知乙烷的结构式如图所示,你从中可获取的信息有(至少写四点):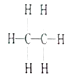
(1)该物质的化学式为。
(2)
(3)
(4)
【答案】
(1)C2H6
(2)乙烷由碳元素和氢元素组成
(3)乙烷中碳氢原子个数比为1:3
(4)一个乙烷分子由两个碳原子和6个氢原子构成
【解析】化学式的意义:①宏观意义:a.表示一种物质; b.表示该物质的元素组成; ②微观意义:a.表示该物质的一个分子; b.表示该物质的分子构成; ③量的意义:a.表示物质的一个分子中各原子个数比; b.表示组成物质的各元素质量比。(1)由题中信息可知,一个分子中有2个碳原子、6个氢原子,所以该物质的化学式为C2H6;(2) 乙烷由碳元素和氢元素组成; (3) 乙烷中碳氢原子个数比为1:3 ; (4) 一个乙烷分子由两个碳原子和6个氢原子构成。(乙烷中碳元素和氢元素的质量比为:2×12:6=4:1)。
所以答案是:C2H6;乙烷由碳元素和氢元素组成;乙烷中碳氢原子个数比为1:3;一个乙烷分子由两个碳原子和6个氢原子构成。

 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案【题目】医用CaCl2·2H2O可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用CaCl2·2H2O的工艺流程为:
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
开始沉淀时的pH | 2.3 | 4.0 | 7.8 |
完全沉淀时的pH | 3.7 | 5.2 | 10.8 |
(1)在实验室进行溶解时玻璃棒的作用是 , 过滤时用到的玻璃仪器有烧杯、玻璃棒、。
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是;滤渣A的主要成分的化学式为。
(3)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少 ?(写出计算过程)
(4)酸化时加盐酸的主要目的为了 。
【题目】某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”感到非常好奇,设计实验进行探究。
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【查阅资料】① 人呼出的气体中主要成分是N2、O2、CO2和水蒸气等。
②CO2 + 2NaOH=Na2CO3 + H2O。
③碳酸钙和稀盐酸反应生成二氧化碳、水和氯化钙。
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
(1)【进行实验】实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
实验操作如下图所示。
实验现象及结论:观察到现象,判断过氧化钠与氮气没有发生反应。
(2)实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
同学们在老师的指导下设计了如下图所示装置:
其中A装置的作用是 , 发生的变化是变化。
实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气。
(3)实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。
同学们在老师的指导下设计了如下图所示装置。
实验记录
实验操作 | 主要实验现象 | 实验结论及解释 | |
① | 检查装置的气密性。 | 装置的气密性良好。 | |
② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸。 | A装置中观察到的现象有 , C装置中有气泡出现。 | A装置中发生反应的符号式为; |
③ | 一段时间后用带火星的木条在D内进行检验。 | 带火星的木条复燃。 | 过氧化钠与二氧化碳反应并生成氧气。 |
(4)【实验反思】
①根据实验Ⅱ和Ⅲ,过氧化钠与二氧化碳或水蒸气反应后,还产生了另一种物质,该物质是(填“单质”或“化合物”)。
②某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是 。