题目内容
已知镁条在点燃条件下可以在二氧化碳中燃烧生成氧化镁和黑色的碳粒,此反应的化学方程式为 ,在该反应中,镁、二氧化碳、氧化镁、碳四种物质的质量比为 ,该反应中氧化剂是 .
考点:书写化学方程式、文字表达式、电离方程式,常见化学反应中的质量关系
专题:化学用语和质量守恒定律
分析:根据题意,镁条在点燃条件下可以在二氧化碳中燃烧生成氧化镁和黑色的碳粒,写出此反应的化学方程式、利用各物质之间的质量比等于相对分子质量和的比,进行分析解答.
解答:解:镁条在点燃条件下可以在二氧化碳中燃烧生成氧化镁和黑色的碳粒,此反应的化学方程式为:2Mg+CO2
C+2MgO.
2Mg+CO2
C+2MgO
48 44 12 80
在该反应中,镁、二氧化碳、氧化镁、碳四种物质的质量比48:44:80:12=12:11:20:3.
该反应中二氧化碳提供了氧,发生了还原反应,在该反应中做氧化剂.
故答案为:2Mg+CO2
C+2MgO;12:11:20:3;二氧化碳.
| ||
2Mg+CO2
| ||
48 44 12 80
在该反应中,镁、二氧化碳、氧化镁、碳四种物质的质量比48:44:80:12=12:11:20:3.
该反应中二氧化碳提供了氧,发生了还原反应,在该反应中做氧化剂.
故答案为:2Mg+CO2
| ||
点评:本题难度不大,主要考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下面是对“2”的含义的解释,其中错误的是( )
| A、Fe2+:一个亚铁离子带2个单位正电荷 |
| B、Ba(OH)2:氢氧化钡中,钡离子和氢氧根离子的个数比是1:2 |
| C、Mg2+:带2个单位正电荷的镁离子 |
| D、2SO42-:2个硫酸根离子,每个硫酸根离子带2个单位负电荷 |
将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X.测得反应前后物质的质量如下表:
下列判断正确的是( )
| 物 质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A、表中m的值为2.8 |
| B、X可能是该反应的催化剂 |
| C、减少氧气的量可以减少X的生成 |
| D、物质X一定含有碳元素,可能含有氢元素 |
如图为初中化学常见气体的发生装置与收集装置,有关这些装置的说法不正确的是( )
A、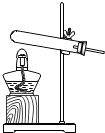 如图装置可作为加热固体制取气体的发生装置 |
B、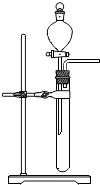 如图装置中分液漏斗的作用是方便添加液体药品 |
C、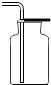 如图装置可用于收集H2、CO2 |
D、 如图装置可用于收集H2、O2 |

 某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.
某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.
 如图是铁丝在氧气中燃烧的实验,回答下列问题:
如图是铁丝在氧气中燃烧的实验,回答下列问题: