题目内容
(2010?江西)将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量与反应时间的关系如图.关于甲、乙两金属判断合理的是( )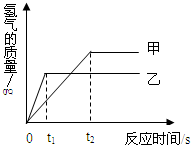

分析:根据金属和酸溶液反应的图象可以得出:①得到的氢气的多少②金属的活动性强弱:反应过程需要的时间越短说明该金属的活动性越强③如果这两种金属元素在化合物中的化合价相同,根据氢气的多少可以判断金属的相对原子质量的大小:相对原子质量越大的得到的氢气越少,相对原子质量越小的得到的氢气越多.从图象中不难看出:两种金属元素在化合物中的化合价相同,甲的相对原子质量比乙的相对原子质量小;金属乙的反应需要的时间短,说明金属乙的反应速率快,即金属乙的金属活动性强,金属乙比甲活泼.
解答:解:A、因铁的相对原子质量比镁的相对原子质量大;故错
B、因锌的相对原子质量比镁的相对原子质量大;故错
C、锌的金属性比铁活泼,不符合题意;故错
D、铁的金属性比锌弱,铁的相对原子质量比锌的相对原子质量小;故对
故选D
B、因锌的相对原子质量比镁的相对原子质量大;故错
C、锌的金属性比铁活泼,不符合题意;故错
D、铁的金属性比锌弱,铁的相对原子质量比锌的相对原子质量小;故对
故选D
点评:主要考查了金属和酸溶液的反应的图象从中可以得到什么样的信息,从而培养学生分析问题、解决问题的能力,加强学生对金属活动性顺序的理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
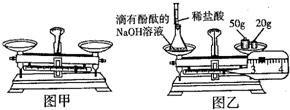 (2010?江西)下图是某班同学验证质量守恒定律实验的片段.
(2010?江西)下图是某班同学验证质量守恒定律实验的片段.